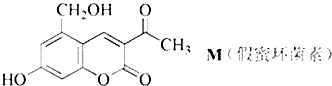
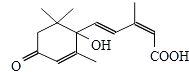
题目内容
【题目】用如图所示实验装置(夹持仪器已略去)探索铜丝与过量浓硫酸反应的产物,下列有关说法正确的是
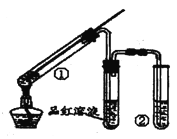
A. 品红溶液的作用是吸收SO2,防止污染空气
B. 试管②中盛放的试剂通常是NaOH溶液
C. 试管①中有白色固体生成,向①中加水后溶液呈蓝色
D. 该反应中浓硫酸既表现了强氧化性,又表现了酸性
【答案】BD
【解析】试题分析:A.SO2具有漂白性,品红能被二氧化硫漂白,可用品红溶液验证SO2的生成,试管②中的溶液才是吸收SO2,防止污染空气,A项错误;B. SO2有毒,不能释放到空气中,SO2是酸性氧化物,能与强碱反应,所以试管②中盛放的试剂通常是NaOH溶液,B项正确;C. 铜与浓硫酸反应生成硫酸铜、SO2和水,实验中,铜丝与过量浓硫酸的反应生成是硫酸铜,试管中含有大量水,不会生成白色固体,CuSO4溶液呈蓝色,为确认CuS04生成,无须向①中加水,C项错误;D.该反应有硫酸铜生成,表现了浓硫酸的酸性,有SO2生成,表现了浓硫酸的强氧化性,D项正确;答案选BD。

 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案【题目】某化学小组采用类似制乙酸乙酯的装置(如图1),以环己醇制备环己烯.
已知: ![]()
密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
环己醇 | 0.96 | 25 | 161 | 能溶于水 |
环己烯 | 0.81 | ﹣103 | 83 | 难溶于水 |
(1)制备粗品将12.5mL环己醇加入试管A中,再加入1mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品.
①A中碎瓷片的作用是 , 导管B除了导气外还具有的作用是 .
②试管C置于冰水浴中的目的是 .
(2)制备精品①环己烯粗品中含有环己醇和少量酸性杂质等.加入饱和食盐水,振荡、静置、分层,环己烯在层(填“上”或“下”),分液后用(填选项字母)洗涤.
a.KMnO4溶液 b.稀硫酸 c.Na2CO3溶液
②再将环己烯按如图2装置蒸馏,冷却水从进入.蒸馏时要加入生石灰,目的是 .
③收集产品时,控制的温度应在左右,实验制得的环己烯精品质量低于理论产量,可能的原因是(填选项字母).
a.蒸馏时从70℃开始收集产品
b.环己醇实际用量多了
c.制备粗品时环己醇随产品一起蒸出
(3)以下区分环己烯精品和粗品的方法,合理的是(填选项字母).a.用酸性高锰酸钾溶液 b.用金属钠 c.用溴水 d.测定沸点.
【题目】下述实验中均有红棕色气体产生,对比分析所得结论不正确的是( )
|
|
|
① | ② | ③ |
A. 由①中的红棕色气体,推断产生的气体一定是混合气体
B. 红棕色气体不能表明②中木炭与浓硝酸产生了反应
C. 由③说明浓硝酸具有挥发性,生成的红棕色气体为还原产物
D. ③的气体产物中检测出CO2,由此说明木炭一定与浓硝酸发生了反应