题目内容
(2012?山东模拟)现有部分前四周期元素的性质或原子结构如下表:
(1)B单质分子中,含有
(2)若C是固体,C单质的熔点
(3)写出元素D基态原子的电子排布式:
| 元素编号 | 元素性质或原子结构 |
| A | 第三周期中的半导体材料 |
| B | L层s电子数比p电子数少1 |
| C | 属于第二周期,原子中有2个未成对电子 |
| D | 前四周期呀中其未成对电子数最多 |
1
1
个σ键和2
2
个π键,元素B的气态氢化物的空间型为三角锥型
三角锥型
.(2)若C是固体,C单质的熔点
高于
高于
A单质的熔点(填“高于”或“低于”),若C的单质是气体,A与C形成的化合的晶体类型是原子晶体
原子晶体
.(3)写出元素D基态原子的电子排布式:
1s22s22p63s23p63d54s1
1s22s22p63s23p63d54s1
.分析:A是第三周期中的半导体材料,故A为Si元素;B元素原子L层s电子数比p电子数少1,则外围电子排布为2s22p3,故B为氮元素;C属于第二周期,原子中有2个未成对电子,则外围电子排布为2s22p2,或则外围电子排布为2s22p4,故C为碳元素或氧元素;前四周期中其未成对电子数最多,则外围电子排布为3d54s1,核外电子数为24,为Cr元素,据此解答.
解答:解:A是第三周期中的半导体材料,故A为Si元素;B元素原子L层s电子数比p电子数少1,则外围电子排布为2s22p3,故B为氮元素;C属于第二周期,原子中有2个未成对电子,则外围电子排布为2s22p2,或则外围电子排布为2s22p4,故C为碳元素或氧元素;前四周期中其未成对电子数最多,则外围电子排布为3d54s1,核外电子数为24,D为Cr元素,
(1)氮气分子中氮原子之间形成N≡N三键,含有1个σ键、2个π键,元素B的气态氢化物为NH3,分子中氮原子成3个N-H键,氮原子含有1对孤对电子,故为三角锥型,
故答案为:1;2;三角锥型;
(2)若C是固体,则C为碳元素,C-C键键长小于Si-Si键键长,故碳的单质熔点高于硅单质.若C的单质是气体,则C为氧元素,氧气与硅形成的化合物二氧化硅属于原子晶体,故答案为:高于;原子晶体;
(3)D为Cr元素,外围电子排布为3d54s1,则Cr元素基态原子的电子排布式:1s22s22p63s23p63d54s1,故答案为:1s22s22p63s23p63d54s1.
(1)氮气分子中氮原子之间形成N≡N三键,含有1个σ键、2个π键,元素B的气态氢化物为NH3,分子中氮原子成3个N-H键,氮原子含有1对孤对电子,故为三角锥型,
故答案为:1;2;三角锥型;
(2)若C是固体,则C为碳元素,C-C键键长小于Si-Si键键长,故碳的单质熔点高于硅单质.若C的单质是气体,则C为氧元素,氧气与硅形成的化合物二氧化硅属于原子晶体,故答案为:高于;原子晶体;
(3)D为Cr元素,外围电子排布为3d54s1,则Cr元素基态原子的电子排布式:1s22s22p63s23p63d54s1,故答案为:1s22s22p63s23p63d54s1.
点评:本题考查结构性质位置关系、分子结构与化学键、晶体类型与性质、核外电子排布规律等,难度不大,注意基础知识的理解掌握.

练习册系列答案
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案
相关题目
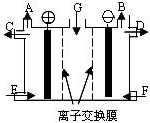 (2012?山东模拟)现有用离子交换膜(只允许对应的离子通过)和石墨作电极的电解槽电解饱和的Na2SO4溶液生产NaOH和H2SO4,下列说法中正确的是( )
(2012?山东模拟)现有用离子交换膜(只允许对应的离子通过)和石墨作电极的电解槽电解饱和的Na2SO4溶液生产NaOH和H2SO4,下列说法中正确的是( )