题目内容
【题目】实验室需要0.1molL﹣1 NaOH溶液450mL.回答下列问题: 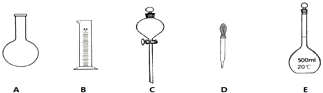
(1)如图所示的仪器中配制溶液肯定不需要的是(填序号),配制上述溶液还需用到的玻璃仪器是(填仪器名称).
(2)在配制NaOH溶液时:
①根据计算用托盘天平称取NaOH的质量为g;
②若NaOH溶液在转移至容量瓶时,洒落了少许,则所得溶液浓度0.1mol/L(填“>”、“<”或“=”);
③若NaOH固体溶解后立即移入容量瓶→洗烧杯→洗涤液移入容量瓶→定容,则所得溶液浓度0.1molL﹣1(填“>”、“<”或“=”).
【答案】
(1)AC;烧杯、玻璃杯
(2)2.0;<;>
【解析】解:(1)配制该溶液需要用到的玻璃仪器为:量筒、烧杯、玻璃棒、胶头滴管、容量瓶,所以不需要为仪器为AC;还缺少的玻璃仪器为:烧杯和玻璃杯,所以答案是:AC;烧杯、玻璃棒;(2)①因无450 mL的容量瓶,配制NaOH溶液要用500 mL的容量瓶,m(NaOH)=cVM=0.1 molL﹣1×0.5 L×40 gmol﹣1=2.0 g,所以答案是:2.0;②若NaOH溶液在转移至容量瓶时,洒落了少许,则所得溶液中溶质的物质的量偏小,溶液浓度偏低,小于0.1mol/L,所以答案是:<;③NaOH溶于水放出大量热,应把它冷却至室温后再移入容量瓶中,否则定容后,溶液冷却到室温后,体积减小,浓度偏高,所以答案是:>.

【题目】某研究性学习小组为了探究醋酸的电离情况,进行了如下实验:
【实验一】配制并标定醋酸溶液的浓度。取冰醋酸配制250 mL 0.2 mol·L-1的醋酸溶液,然后用0.2 mol·L-1的醋酸溶液稀释成所需浓度的溶液,再用NaOH标准溶液对所稀释的醋酸溶液的浓度进行标定。请回答下列问题:
(1)配制250 mL 0.2 mol·L-1醋酸溶液时需要用到的玻璃仪器有量筒、烧杯、玻璃棒、__________。
(2)为标定某醋酸溶液的准确浓度,用0.200 0 mol·L-1的NaOH溶液对20.00 mL醋酸溶液进行滴定,几次滴定消耗NaOH溶液的体积如下:
实验序号 | 1 | 2 | 3 | 4 |
消耗NaOH溶液 的体积(mL) | 20.05 | 20.00 | 18.40 | 19.95 |
则①滴定时选用________(A.石蕊 B.酚酞 C.不用指示剂 D.甲基橙)为指示剂(填字母)
②该醋酸溶液的准确浓度为________(保留小数点后四位)。
【实验二】探究浓度对醋酸电离程度的影响。用pH计测定25 ℃时不同浓度的醋酸溶液的pH,结果如下:
醋酸浓度 (mol·L-1) | 0.001 0 | 0.010 00 | 0.020 0 | 0.100 0 | 0.200 0 |
pH | 3.88 | 3.38 | 3.23 | 2.88 | 2.83 |
(3)根据表中数据,可以得出醋酸是弱电解质的结论,你认为得出此结论的依据是_________________。
(4)从表中的数据,还可以得出另一结论:随着醋酸浓度的减小,醋酸的电离程度______(填“增大”“减小”或“不变”)。
【实验三】探究温度对醋酸电离程度的影响。
(5)要完成该探究,需要用pH计(或pH试纸)测定 ___________________________。
【醋酸电离的应用】
(6)通过实验测定常温下醋酸的Ka=1×10-5,则0.1 mol·L-1醋酸钠溶液的pH=________。
【题目】【宁夏六盘山高级中学2017届高三第四次模拟考试】由下列事实得出的结论正确的是
事 实 | 结 论 | |
A | HClO与H2SO3反应生成H2SO4和HCl | 非金属性:Cl>S |
B | N2比白磷稳定得多 | 非金属性:N<P |
C | 在约800℃时,金属钠可从熔融的KCl中置换出K | 金属性:Na>K |
D | 工业上电解Na3AlF6和Al2O3的熔融混合物得到Al | 金属活动性:Na>Al |