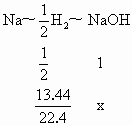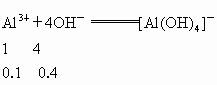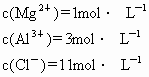题目内容
有一块金属钠投入盛有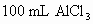 和
和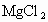 混合溶液的烧杯中,发现烧杯中沉淀先多后少,反应完毕后收集到标准状况下
混合溶液的烧杯中,发现烧杯中沉淀先多后少,反应完毕后收集到标准状况下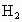 共13.44L,同时得到21.4 g沉淀.将此沉淀溶于过量苛性钠溶液中,发现沉淀减轻了15.6g.求原溶液中
共13.44L,同时得到21.4 g沉淀.将此沉淀溶于过量苛性钠溶液中,发现沉淀减轻了15.6g.求原溶液中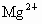 、
、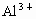 、
、 的物质的量浓度分别为______mol/L、
__________mol/L、 __________mol/L.
的物质的量浓度分别为______mol/L、
__________mol/L、 __________mol/L.
答案:1,3,11
解析:
解析:
|
(1) 由题知,生成沉淀先多后少,则溶液中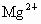 沉淀完全, 沉淀完全, 有部分转为 有部分转为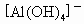 .设总的钠产生的NaOH的物质的量为x,则由 .设总的钠产生的NaOH的物质的量为x,则由
解得 x=1.2 mol(2) 加入过量NaOH后,生成的沉淀 全是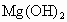 . .
第一次沉淀中 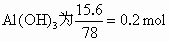 ,产生此 ,产生此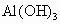 沉淀消耗NaOH为0.6 mol. 沉淀消耗NaOH为0.6 mol.
( 3)由上表明,第一次沉淀时,有1.2-0.2-0.6=0.4 mol NaOH参与下列反应:
所以总共有 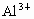 为0.3 mol相应的 为0.3 mol相应的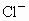 应有0.1×2+0.3×3=1.1 mol 应有0.1×2+0.3×3=1.1 mol
所以原溶液中:
|

练习册系列答案
 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案
相关题目