题目内容
(2011?深圳模拟)已知:5FeS2+14CuSO4+12H2O=7Cu2S+5FeSO4+12H2SO4,下列说法正确的是( )
分析:从化合价的角度来判断氧化产物、被氧化的元素等问题,计算转移电子总数可按化合价升高总数或化合价降低总数来确定.
解答:解:分析反应 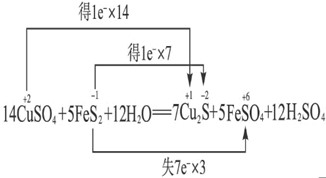 可知,
可知,
A、CuSO4中Cu的化合价降低生成Cu2S,FeS2中S的化合价也降低生成Cu2S,故被还原的元素有Cu和S,Cu2S只是还原产物,非氧化产物,故A错误;
B、由反应可知5molFeS2发生反应,有3mol×7=21 mol电子转移,故B正确;
C、由分析可知,Cu、S元素的化合价降低,则被还原的元素有有Cu和S,故C错误;
D、产物中SO42- 有一部分是氧化产物,另一部分由CuSO4提供,故D错误;
故选B.
 可知,
可知,A、CuSO4中Cu的化合价降低生成Cu2S,FeS2中S的化合价也降低生成Cu2S,故被还原的元素有Cu和S,Cu2S只是还原产物,非氧化产物,故A错误;
B、由反应可知5molFeS2发生反应,有3mol×7=21 mol电子转移,故B正确;
C、由分析可知,Cu、S元素的化合价降低,则被还原的元素有有Cu和S,故C错误;
D、产物中SO42- 有一部分是氧化产物,另一部分由CuSO4提供,故D错误;
故选B.
点评:本题考查了氧化产物的判断,被还原元素及氧化还原的实质.本题易错选C,漏掉了被还原的S元素,也易错选D,不清楚SO42- 有一部分是氧化产物,另一部分由CuSO4提供.从化合价的角度掌握氧化还原的有关概念是解答此类题目的关键.

练习册系列答案
 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案
相关题目