题目内容
在2Na2O2+2CO2═2Na2CO3+O2反应中,
(1)用双线桥法标出电子转移的方向和数目______.
(2)______是还原剂,______是氧化剂.
(3)若转移3mol电子,则所产生的氧气在标准状况下的体积为______.
(1)用双线桥法标出电子转移的方向和数目______.
(2)______是还原剂,______是氧化剂.
(3)若转移3mol电子,则所产生的氧气在标准状况下的体积为______.
(1)在 2Na2O2+2CO2═2Na2CO3+O2反应中,只有Na2O2中O元素的化合价发生变化,分别由-1价变化为0价和-2价,用双线桥法可表示为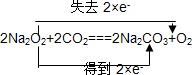 ,故答案为:
,故答案为: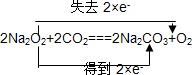 ;
;
(2)只有Na2O2中O元素的化合价发生变化,反应中Na2O2既是氧化剂又是还原剂,故答案为:Na2O2;Na2O2;
(3)由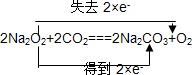 可知若转移3mol电子,则所产生的氧气为1.5mol,体积为1.5mol×22.4L/mol=33.6L,故答案为:33.6L.
可知若转移3mol电子,则所产生的氧气为1.5mol,体积为1.5mol×22.4L/mol=33.6L,故答案为:33.6L.
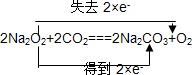 ,故答案为:
,故答案为: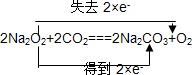 ;
;(2)只有Na2O2中O元素的化合价发生变化,反应中Na2O2既是氧化剂又是还原剂,故答案为:Na2O2;Na2O2;
(3)由
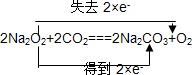 可知若转移3mol电子,则所产生的氧气为1.5mol,体积为1.5mol×22.4L/mol=33.6L,故答案为:33.6L.
可知若转移3mol电子,则所产生的氧气为1.5mol,体积为1.5mol×22.4L/mol=33.6L,故答案为:33.6L.
练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2013年诺贝尔化学奖授予美国科学家马丁·卡普拉斯、迈克尔·莱维特、阿里耶·瓦谢勒,以表彰他们“在开发多尺度复杂化学系统模型方面所做的贡献”。这种用电脑取代木棒作试验模型,催生了现代化学研究手段的一次新飞跃。下列不属于现代化学对物质结构进行研究的手段的是( )
| A.X射线 | B.天平 | C.质谱 | D.核磁共振 |
1999年度诺贝尔化学奖授予了开创“飞秒(10-15s)化学”新领域的科学家,使运用激光光谱技术观测化学反应时分子中原子运动成为可能。你认为该技术不能观察到的是
| A.原子中原子核的内部结构 | B.化学反应中原子的运动 |
| C.化学反应中生成物分子的形成 | D.化学反应中反应物分子的分解 |