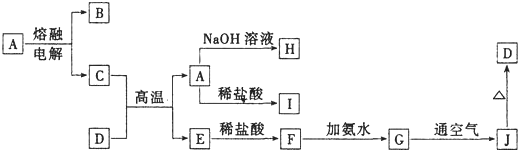
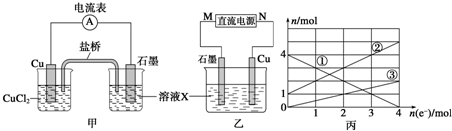
题目内容
正确书写离子方程式时,应使等号两边( )
| A、离子的物质的量相等 |
| B、微粒的总的数量应相等 |
| C、正电荷和负电荷总数应相等 |
| D、电荷量和各元素原子的物质的量应相等 |
考点:离子方程式的书写
专题:离子反应专题
分析:离子方程式的书写规则的第④步“查”:检查式子两边的各种原子的个数及电荷数是否相等、转移电子数是否相等.
解答:
解:书写离子方程式时,等号两边的各元素原子个数、电荷数、转移电子必须相等,既遵循原子守恒和电荷守恒.如2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,表示硫酸和强碱氢氧化钡反应的离子方程式,是正确的,但等号两边离子的物质的量、微粒的总的数量、正电荷和负电荷总数均不一定相等,故ABC错误,
故选D.
故选D.
点评:本题主要考查离子方程式的概念、书写方法和判断规律,明确离子方程式中“=”的含义,知道方程式中都存在哪些物理量相等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
某化学课外活动小组,进行关于溶液中离子检验的探索性实验.下列是A、B、C、D四位同学分别对四个不同试样的检验结果.其中合理的是( )
| A、K+、H+、SO42-、OH- |
| B、Na+、Ca2+、CO32-、NO3- |
| C、Na+、H+、Cl-、CO32- |
| D、Cu2+、Na+、Cl-、SO42- |
观察下列几个装置示意图,有关叙述正确的是( )
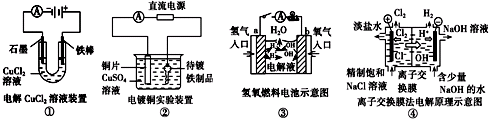

| A、装置①中阳极上析出红色固体 |
| B、装置②的待镀铁制品应与电源负极相连 |
| C、装置③中外电路电子由b极流向a极 |
| D、装置④的离子交换膜允许阳离子、阴离子、水分子自由通过 |
下列说法不正确的是( )
| A、加入苯酚显紫色的溶液:K+、NH4+、Cl-、I-;加入酚酞呈红色的溶液:SO42-、K+、Cl-、HSO3- 分别都不能大量共存(常温下) | ||
B、
| ||
| C、已知:25℃时,Mg(OH)2的kSP=5.61×10-12,MgF2的kSP=7.42×10-11,25℃时,在Mg(OH)2的悬浊液中加入NaF溶液后,Mg(OH)2 可以转化为MgF2 | ||
D、表示H2燃烧热的化学方程式为:H2(g)+
|
230Th和232Th是90号元素钍的两种同位素,232Th可以转化成233U.下列有关Th的说法正确的是( )
| A、230Th的中子数比核外电子数多140 |
| B、230Th和232Th的化学性质相同 |
| C、232Th转换成233U是化学变化 |
| D、Th元素的相对原子质量是231 |
现有物质的量浓度为0.1mol/L的盐酸和0.1mol/L的氨水,下列说法中正确的是( )
| A、用湿润的pH试纸测定两种溶液的pH时,氨水的误差更大 |
| B、若混合后溶液恰好呈中性时:c(Cl-)=c(NH4+)+c(NH3?H2O) |
| C、两溶液等体积混合时,充分反应后:c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| D、恰好反应呈中性时,所需氨水的体积大于盐酸的体积 |
氢镍电池是一种应用广泛的可充电电池,它可以取代会产生镉污染的镉镍电池.氢镍电池的总反应为
H2+NiO(OH)
Ni(OH)2,据此判断,下列叙述中正确的是( )
| 1 |
| 2 |
| 放电 |
| 充电 |
| A、电池放电时,H2是正极 |
| B、电池放电时,镍元素被氧化 |
| C、电池充电时,氢元素被还原 |
| D、电池放电时,电池负极周围溶液的pH不断增大 |