题目内容
下列离子方程式正确的是( )
| A、NH4HCO3溶液与过量NaOH溶液反应:NH4++OH-=NH3↑+H2O |
| B、用惰性电极电解饱和氯化钠溶液:2Cl-+2H+═H2↑+Cl2↑ |
| C、向Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-=2Fe2++I2 |
| D、Na2SO3溶液使酸性KMnO4溶液褪色:5SO32-+6H++2MnO4-=5SO42-+2Mn2++3H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.二者反应生成碳酸钠、水和一水合氨;
B.该反应中还生成氢氧根离子;
C.二者反应生成碘和亚铁离子、NO;
D.二者反应生成硫酸根离子、锰离子和水.
B.该反应中还生成氢氧根离子;
C.二者反应生成碘和亚铁离子、NO;
D.二者反应生成硫酸根离子、锰离子和水.
解答:
解:A.二者反应生成碳酸钠、水和一水合氨,离子方程式为NH4++HCO3-+2OH-=NH3.H2O+H2O+CO32-,故A错误;
B.该反应中还生成氢氧根离子,离子方程式为2Cl-+2H2O
H2↑+Cl2↑+2OH-,故B错误;
C.二者反应生成碘和亚铁离子、NO,离子方程式为12H++Fe3++10I-+3NO3-=Fe2++5I2+3NO↑+6H2O,故C错误;
D.二者反应生成硫酸根离子、锰离子和水,离子方程式为5SO32-+6H++2MnO4-=5SO42-+2Mn2++3H2O,故D正确;
故选D.
B.该反应中还生成氢氧根离子,离子方程式为2Cl-+2H2O
| ||
C.二者反应生成碘和亚铁离子、NO,离子方程式为12H++Fe3++10I-+3NO3-=Fe2++5I2+3NO↑+6H2O,故C错误;
D.二者反应生成硫酸根离子、锰离子和水,离子方程式为5SO32-+6H++2MnO4-=5SO42-+2Mn2++3H2O,故D正确;
故选D.
点评:本题考查了离子方程式正误判断,明确物质之间的反应及离子方程式书写规则是解本题关键,注意不能漏写、多写离子反应,易错选项是C,注意:硝酸根离子也能被碘离子还原,为易错点.

练习册系列答案
相关题目
下列说法正确的是( )
| A、硫酸钡难溶于水,其水溶液导电能力极弱,所以硫酸钡是弱电解质 |
| B、CO2溶于水得到的溶液能导电,所以CO2是电解质 |
| C、强电解质溶液的导电能力不一定比弱电解质溶液的导电能力强 |
| D、某物质若不是电解质,就一定是非电解质 |
下列说法正确的是( )
| A、100℃时,纯水中c(H +)=1×10-6mol?L-1,此时纯水显酸性 | ||
| B、25℃时,pH=10的氨水与pH=4盐酸等体积混合,所得溶液呈酸性 | ||
| C、25℃时,将pH=a的醋酸溶液稀释10倍后,溶液的pH=b,则b=(a+1) | ||
D、25℃时,
|
由于易被空气中的氧气氧化而不能长期存放在敞口容器中的是( )
| A、浓盐酸 |
| B、硫酸亚铁(FeSO4)溶液 |
| C、NaOH溶液 |
| D、过氧化纳(Na2O2) |
相关城市空气污染的首要污染物是( )
| A、二氧化硫 | B、二氧化氮 |
| C、二氧化碳 | D、可吸入颗粒物 |
下列实验与对应示意图的关系正确的是( )
| A | B | C | D |
| NaAlO2溶液中逐滴滴加盐酸至过量 | AlCl3溶液中逐滴滴加氨水至过量 | 明矾溶液中逐滴滴加Ba(OH)2溶液至过量 | 澄清石灰水中缓慢通入CO2至过量 |
 |  |  | 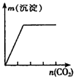 |
| A、A | B、B | C、C | D、D |
 某同学在研究前18号元素时发现,可以将它们排成如图所示的蜗牛形状,图中每个点代表-种元素,其中O点代表氢元素.下列说法中正确的是( )
某同学在研究前18号元素时发现,可以将它们排成如图所示的蜗牛形状,图中每个点代表-种元素,其中O点代表氢元素.下列说法中正确的是( )| A、离0点越远的元素原子半径越大 |
| B、虚线相连的元素处于同一族 |
| C、B、C最高价氧化物的水化物不能相互反应 |
| D、A、B组成的化合物中不可能含有共价键 |
化学世界是个五彩缤纷的世界,下列关于颜色的变化叙述正确的是( )
| A、向盛有苯酚溶液的试管中滴入FeCl3溶液,溶液呈紫色 |
| B、淀粉溶液遇碘离子变蓝 |
| C、氨气能使湿润的蓝色石蕊试纸变红 |
| D、二氧化硫能使石蕊溶液变红后褪色 |
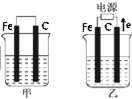 I.C2H6在氧气中完全燃烧生成二氧化碳和液态水,利用该反应设计一个燃料电池,用氢氧化钾溶液作电解质溶液,多孔石墨做电极,在电极上分别通入乙烷和氧气.通入乙烷气体的电极上发生的电极反应式是
I.C2H6在氧气中完全燃烧生成二氧化碳和液态水,利用该反应设计一个燃料电池,用氢氧化钾溶液作电解质溶液,多孔石墨做电极,在电极上分别通入乙烷和氧气.通入乙烷气体的电极上发生的电极反应式是