题目内容
在通常条件下,下列各组物质的性质排列正确的是( )
| A.熔点:CO2>H2O2>SiO2 | B.酸性:HClO>H2SO3>H2CO3 |
| C.沸点:乙烷>戊烷>丁烷 | D.热稳定性:HF>H2O>NH3 |
D
解析试题分析:A、SiO2是原子晶体,熔点最高,CO2和H2O2都是分子晶体,但H2O2是液体,熔点比CO2高,错误;B、H2SO3>H2CO3>HClO,错误;C、结构和性质相似的分子晶体,相对分子质量越大,沸点越高,戊烷>丁烷>乙烷,错误;D、非金属性越强,其对应的非金属氢化物越稳定,同一周期,从左到右,非金属性逐渐增强,HF>H2O>NH3,正确。
考点:考查元素周期律的应用

练习册系列答案
相关题目
元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示, 其中R单质在暗处与H2剧烈化合并发生爆炸。则下列判断正确的是
| A.非金属性:Z<T<X |
| B.R与Q的电子数相差26 |
| C.气态氢化物稳定性:R <T<Q |
| D.最高价氧化物的水化物的酸性: X > T |
Rn+离子有m个电子,它的质量数为A,则原子核内的中子数为 ( )
| A.m +n | B.A-m+n | C.A-m-n | D.A+m-n |
实际存在的11H、12H、13H 、H+和H2,它们是
| A.氢的五种同位素 | B.氢元素的五种不同微粒 | C.氢的五种核素 | D.五种氢元素 |
由短周期元素组成的甲、乙、丙、丁四种物质分别含有两种以上元素,它们的分子质子总数均与氩原子相同。已知甲是气态氢化物,在水中分步电离出两种阴离子。下列推断合理的是 ( )
| A.某钠盐溶液含甲电离出的阴离子,则该溶液显碱性,只能与酸反应 |
| B.乙与氧气的摩尔质量相同,则乙一定含有极性键和非极性键 |
| C.丙中含有第二周期IV A族的元素,则丙一定是甲烷的同系物 |
| D.丁和甲中各元素质量比相同,则丁中一定含有-1价的元素 |
某元素X核电荷数小于18,其原子的电子层数为n,最外层电子数为2n+1,原子核内质子数是2n2-1。下列有关X的说法中,不正确的是 ( )
| A.X能形成化学式为X(OH)3的碱 |
| B.X能形成化学式为NaXO3的含氧酸钠盐 |
| C.X原子的最外层电子数和核电荷数不可能为偶数 |
| D.X能与某些金属元素或非金属元素形成化合物 |
五种短周期元素X、Y、Z、W、Q(X、Y、Z、W、Q分别代表元素符号)在周期表中的位置如图所示。下列说法中,不正确的是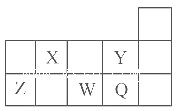
| A.X的气态氢化物与Q的气态氢化物相遇会产生白烟 |
| B.元素的非金属性:Y>Q,同浓度的氢化物水溶液的酸性:HY<HQ |
| C.形成简单离子的半径从小到大的顺序是:Y- <Q- <W2- |
| D.Z的最高价氧化物可溶于水,也能溶于强碱溶液 |