题目内容
【题目】下列实验装置不能达到实验目的的是

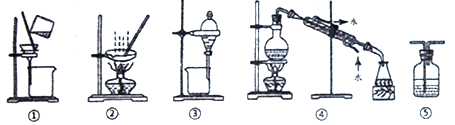
A.用装置A来做SO2的喷泉实验
B.用装置B来验证浓H2SO4与水混合的热量变化
C.用装置C来验证NH3易溶于水
D.用装置D来验证氧化性:Cl2>Br2>I2
【答案】D
【解析】
试题分析:A.SO2是酸性氧化物,与NaOH发生反应:SO2+2NaOH=Na2SO3+H2O,使烧瓶中气体压强减小,烧杯中的NaOH溶液在大气压强的作用下进入烧瓶,由于会不断形成压强差,所以可以用装置A来做SO2的喷泉实验,正确;B.浓硫酸有吸水性,与水接触,放出大量的热,使试管中的空气受热膨胀,U形管内的红墨水左侧液面下降,右侧液面上升,因此用装置B来验证浓H2SO4与水混合的热量变化,正确。C.若氨气极容易溶于水,会使烧瓶中气体的压强减小,小气球内侧与外接大气相通,在大气压强的作用下,小气球鼓起胀大。因此用装置C来验证NH3易溶于水,正确。D.由于元素的非金属性Cl>Br,所以会发生反应:Cl2+2NaBr=2NaCl+Br2。反应产生的Br2通入到KI溶液中,发生反应:2KI+ Br2=2KBr+I2,I2使淀粉溶液变为蓝色。同时为反应的Cl2与KI也发生反应:2KI+ Cl2=2KCl+I2,I2使淀粉溶液变为蓝色。因此不能证明氧化性:Cl2>Br2>I2,错误。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
【题目】下面是某个品牌的食用碘盐包装上的标签。下列关于此标签的说法中正确的是( )
配料 | 精盐、碘酸钾、抗结剂 |
碘含量 | 35±15 mg·kg-1 |
储存方法 | 密封、避光、防潮 |
食用方法 | 烹饪时,待食品熟后加入碘盐 |
A. 高温会导致碘的损失
B. 碘酸钾可氧化氯化钠
C. 可用淀粉检验碘盐中的碘酸钾
D. 该碘盐中碘酸钾的含量为20~50 mg·kg-1