题目内容
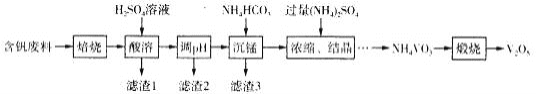
【题目】五氧化二钒(V2O5)在冶金、搪瓷、磁性材料等领域有重要应用。实验室以含钒废料(含V2O3、CuO、MnO、SiO2、A12O3、有机物)为原料制备V2O5的一种流程如图:
已知I.含钒离子在溶液中的主要存在形式与溶液pH的关系如表所示:

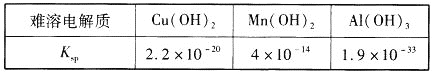
Ⅱ.25℃时,难溶电解质的溶度积常数如表所示:
Ⅲ.NH4VO3在水中的溶解度:20℃、4.8g·L-1;60℃、24.2g·L-1。
回答下列问题:
(1)“焙烧”的目的是_____。
(2)“滤渣1”的用途为____(写出一种即可)。
(3)通过计算说明,常温下,若“调pH”为7,Cu2+是否沉淀完全____。(溶液中离子浓度小于10-5mol·L-1时,认为该离子沉淀完全)
(4)“沉锰”需将温度控制在70℃左右,温度不能过高或过低的原因为____。
(5)结晶所得NH4VO3需进行洗涤、干燥。合适的洗涤试剂为____;证明NH4VO3已洗涤干净的实验操作及现象为____。
(6)“煅烧”时生成两种能参与大气循环的气体,该反应的化学方程式为_____。
【答案】除去有机物杂质,将V2O3氧化为V2O5 制光导纤维、制玻璃、制硅胶 “调节pH”为7,溶液中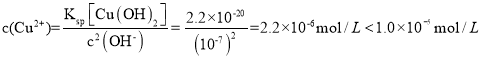 ,Cu2+沉淀完全; 温度过低,反应速率慢,NH4VO3可能提前结晶析出导致产率低;温度过高,NH4HCO3分解导致原料利用率低 冷水 取少量最后一次洗涤液于洁净试管中,滴加BaCl2溶液,无明显现象,证明NH4VO3已洗涤干净 4NH4VO3+3O2
,Cu2+沉淀完全; 温度过低,反应速率慢,NH4VO3可能提前结晶析出导致产率低;温度过高,NH4HCO3分解导致原料利用率低 冷水 取少量最后一次洗涤液于洁净试管中,滴加BaCl2溶液,无明显现象,证明NH4VO3已洗涤干净 4NH4VO3+3O2 ![]() 2V2O5+2N2+8H2O
2V2O5+2N2+8H2O
【解析】
(1)含钒废料中含有有机物杂质,焙烧时会被除去,V2O5是由V2O3制备的,根据V元素化合价的变化分析;
(2)SiO2不与硫酸反应,判断“滤渣1”为SiO2,再写出其用途;
(3)根据溶度积的公式进行计算;
(4)根据温度对反应速率以及对物质的稳定性的影响分析;
(5)根据已知信息NH4VO3的溶解度选择洗涤试剂;检验NH4VO3洗涤干净,只要检验最后一次洗涤液中没有溶液中的硫酸根离子即可;
(6)根据NH4VO3“煅烧”时生成两种能参与大气循环的气体,即产物有V2O5、N2、H2O,据此写出该反应的化学方程式。
(1)焙烧会除去有机物杂质,同时根据V2O3中V元素的化合价为+3价,V2O5中V元素的化合价为+5价知,焙烧还可以将烧V2O3氧化为V2O5;
故答案为:除去有机物杂质,将V2O3氧化为V2O5;
(2)用硫酸酸溶时,SiO2不反应,因此“滤渣1”为SiO2,其用途为制光导纤维、制玻璃、制硅胶等;
故答案为:制光导纤维、制玻璃、制硅胶等(写出一种即可);
(3)调节pH为7,溶液中c(Cu2+)= molL-1=2.2×10-6molL-1<10-5molL-1,Cu2+沉淀完全;
molL-1=2.2×10-6molL-1<10-5molL-1,Cu2+沉淀完全;
故答案为:调节pH为7,溶液中c(Cu2+)= molL-1=2.2×10-6molL-1<10-5molL-1,Cu2+沉淀完全;
molL-1=2.2×10-6molL-1<10-5molL-1,Cu2+沉淀完全;
(4)温度过低,反应速率慢,NH4VO3可能提前结晶析出导致产率低;温度过高,NH4HCO3分解导致原料利用率低;
故答案为:温度过低,反应速率慢,NH4VO3可能提前结晶析出导致产率低;温度过高。NH4HCO3分解导致原料利用率低;
(5)因为NH4VO3在冷水中的溶解度小,在热水中溶解度大,因此选择冷水作洗涤试剂;
若NH4VO3未洗涤干净,则固体上会附着硫酸根离子,因此检验NH4VO3已洗涤干净,只要检验最后一次洗涤液中没有硫酸根离子即可,则实验操作及现象为取少量最后一次洗涤液于洁净试管中,滴加BaCl2溶液,无明显现象,证明NH4VO3已洗涤干净;
故答案为:冷水;取少量最后一次洗涤液于洁净试管中,滴加BaCl2溶液,无明显现象,证明NH4VO3已洗涤干净;
(6)根据“煅烧”时生成两种能参与大气循环的气体,可得该反应的化学方程式为4NH4VO3+3O2![]() 2V2O5+2N2+8H2O;
2V2O5+2N2+8H2O;
故答案为:4NH4VO3+3O2![]() 2V2O5+2N2+8H2O。
2V2O5+2N2+8H2O。

 阅读快车系列答案
阅读快车系列答案