题目内容
现有A、B、C、D四种元素,其原子序数依次递增.已知,A、C为短周期非金属元素,其单质在常温下均为气体,两单质混合见光爆炸生成AC,AC溶液显强酸性.B、D为金属元素,B的原子序数为D的一半,D与C2和AC溶液反应分别得DC3和DC2,烧碱溶液不能与D单质反应,而能与B单质反应.请回答下列问题:
(1)C的原子结构示意图为______;B在周期表中的位置是______.
(2)用电子式表示AC的形成过程______.
(3)写出B单质与NaOH溶液反应的离子方程式______.
(4)电浮选凝聚法是工业上采用的一种污水处理方法,右图是该方法处理污水的实验装置示意图(B、D金属单质作电极).实验过程中,污水的pH始终保持在5.0~6.0之间.接通电源后,阴极产生的气体将污物带到水面形成浮渣而刮去,起到浮选净化作用;阳极产生的沉淀具有吸附性,吸附污物而沉积,起到凝聚净化作用.阳极的电极反应有两个,分别是2H2O-4e-=4H++O2↑和______.阳极区生成沉淀的离子方程式是______.
(5)一定条件下,2mol B与3mol D的氧化物W恰好反应,则W的化学式______.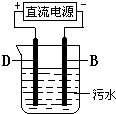
(1)C的原子结构示意图为______;B在周期表中的位置是______.
(2)用电子式表示AC的形成过程______.
(3)写出B单质与NaOH溶液反应的离子方程式______.
(4)电浮选凝聚法是工业上采用的一种污水处理方法,右图是该方法处理污水的实验装置示意图(B、D金属单质作电极).实验过程中,污水的pH始终保持在5.0~6.0之间.接通电源后,阴极产生的气体将污物带到水面形成浮渣而刮去,起到浮选净化作用;阳极产生的沉淀具有吸附性,吸附污物而沉积,起到凝聚净化作用.阳极的电极反应有两个,分别是2H2O-4e-=4H++O2↑和______.阳极区生成沉淀的离子方程式是______.
(5)一定条件下,2mol B与3mol D的氧化物W恰好反应,则W的化学式______.

(1)短周期非金属元素,其单质在常温下为气体有:H2、N2、O2、F2、Cl2,根据题意,A、C两单质混合见光爆炸生成AC,混合见光爆炸是H2和Cl2的特征反应,结合原子序数依次递增,则可确定A是H元素,单质是H2,C是Cl元素,单质是Cl2.化合物AC为HCl.D与C2和AC溶液反应分别得DC3和DC2,即D与Cl2和HCl溶液反应分别得DCl3和DCl2,可分析出金属D化合价具有+2、+3价,确定出D为Fe元素.Fe的原子序数为26,则B的原子序数为13,即B为Al元素.C是Cl,Cl的原子序数=核电荷数=核外电子数=17,故原子示意图为
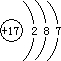
,B是Al,Al的原子序数=13,原子核外有3个电子层,最外层排布3个电子,根据电子层数=周期数,最外层电子数=主族序数,可得Al在周期表中位置为第三周期、第IIIA族,
故答案为:Cl

;第三周期第IIIA族;
(2)AC为化合物HCl,用电子式表示形成过程时,反应物用原子的电子式表示,生成物用化合物的电子式表示,符号用“→”符号,故表示为
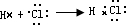
,
故答案为:
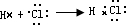
;
(3)B单质是Al,根据铝的性质,与NaOH溶液反应时有水参与,生成偏铝酸钠和氢气,反应为Al+NaOH+H2O→NaAlO2+H2↑,根据化合价升降法配平,Al由0价上升到+3价,上升3价,H2中H由+1价降低为0价,总共降低2价,所以Al前面计量数为2,
H2前面计量数为3,其它物质前计量数根据原子守恒配平即得方程式2Al+2NaOH+2H2O=2NaAlO2+3H2↑,
改写离子方程式时Al、H2是单质保留化学式,H2O是弱电解质保留化学式,NaOH和NaAlO2是易溶于水、易电离物质改成离子形式,再删除不参与离子反应的Na+,
即得离子方程式2Al+2OH-+2H2O=2AlO2-+3H2↑,故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(4)根据题意,电解池的阳极材料为Fe,阴极材料为Al.金属作阳极时,电极称为活性电极,由于金属失电子能力强于溶液中的阳离子,所以阳极上是活性电极自身先失去电子.电解池的阳极放电顺序是:活性电极>Ag+>Hg2+>Fe3+>Cu2+>H+等,因此阳极的另一个电极反应为Fe-2e-=Fe2+.生成的Fe2+进入溶液中,溶液中Fe2++2OH-═Fe(OH)2↓,来自水的电离H2O
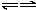
H++OH-,Fe(OH)2易被氧气氧化,反应为4Fe(OH)2+O2+2H2O═4Fe(OH)3↓,上述三步反应合并即得总反应为4Fe2++10H2O+O2=4Fe(OH)3↓+8H+.
故答案为:Fe-2e-=Fe2+;4Fe2++10H2O+O2=4Fe(OH)3↓+8H+;
(5)根据题意,B单质是Al,D为Fe,2molAl与3molFe的氧化物反应为铝热反应,生成Fe和铝的氧化物,依据原子守恒,
2molAl生成1molAl2O3,1molAl2O3中共含有3mol氧原子,3mol氧原子只能来自于3molFe的氧化物中,因此Fe的氧化物中只含一个氧原子,
反应方程式为2Al+3FeO
Al2O3+3Fe,即D的氧化物W为FeO.
故答案为:FeO.

,B是Al,Al的原子序数=13,原子核外有3个电子层,最外层排布3个电子,根据电子层数=周期数,最外层电子数=主族序数,可得Al在周期表中位置为第三周期、第IIIA族,
故答案为:Cl

;第三周期第IIIA族;
(2)AC为化合物HCl,用电子式表示形成过程时,反应物用原子的电子式表示,生成物用化合物的电子式表示,符号用“→”符号,故表示为
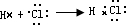
,
故答案为:
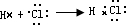
;
(3)B单质是Al,根据铝的性质,与NaOH溶液反应时有水参与,生成偏铝酸钠和氢气,反应为Al+NaOH+H2O→NaAlO2+H2↑,根据化合价升降法配平,Al由0价上升到+3价,上升3价,H2中H由+1价降低为0价,总共降低2价,所以Al前面计量数为2,
H2前面计量数为3,其它物质前计量数根据原子守恒配平即得方程式2Al+2NaOH+2H2O=2NaAlO2+3H2↑,
改写离子方程式时Al、H2是单质保留化学式,H2O是弱电解质保留化学式,NaOH和NaAlO2是易溶于水、易电离物质改成离子形式,再删除不参与离子反应的Na+,
即得离子方程式2Al+2OH-+2H2O=2AlO2-+3H2↑,故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(4)根据题意,电解池的阳极材料为Fe,阴极材料为Al.金属作阳极时,电极称为活性电极,由于金属失电子能力强于溶液中的阳离子,所以阳极上是活性电极自身先失去电子.电解池的阳极放电顺序是:活性电极>Ag+>Hg2+>Fe3+>Cu2+>H+等,因此阳极的另一个电极反应为Fe-2e-=Fe2+.生成的Fe2+进入溶液中,溶液中Fe2++2OH-═Fe(OH)2↓,来自水的电离H2O
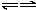
H++OH-,Fe(OH)2易被氧气氧化,反应为4Fe(OH)2+O2+2H2O═4Fe(OH)3↓,上述三步反应合并即得总反应为4Fe2++10H2O+O2=4Fe(OH)3↓+8H+.
故答案为:Fe-2e-=Fe2+;4Fe2++10H2O+O2=4Fe(OH)3↓+8H+;
(5)根据题意,B单质是Al,D为Fe,2molAl与3molFe的氧化物反应为铝热反应,生成Fe和铝的氧化物,依据原子守恒,
2molAl生成1molAl2O3,1molAl2O3中共含有3mol氧原子,3mol氧原子只能来自于3molFe的氧化物中,因此Fe的氧化物中只含一个氧原子,
反应方程式为2Al+3FeO
| ||
故答案为:FeO.

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案
相关题目