题目内容
四只试剂瓶中分别盛装有NaNO3溶液、Na2CO3溶液、Na2SO4溶液和NaCl溶液,在四支试管中分别取四种溶液各1mL,做下列实验.
(1)在四支试管中分别滴入稀HNO3,一支试管内有气体产生,离子方程式是______.
(2)然后在剩余三支试管中分别滴入Ba(NO3)2溶液,一支试管内出现白色沉淀,离子方程式是______.
解:(1)在四支试管中分别滴入稀HNO3,硝酸只能和碳酸钠反应生成二氧化碳气体,原理是:CO32-+2H+=CO2↑+H2O,故答案为:CO32-+2H+=CO2↑+H2O;
(2)NaNO3溶液、Na2SO4溶液和NaCl溶液中,只有Na2SO4溶液和硝酸钡发生复分解反应生成白色沉淀,离子方程式是:SO42-+Ba2+=BaSO4↓,故答案为:SO42-+Ba2+=BaSO4↓.
分析:(1)硝酸和碳酸钠反应生成二氧化碳气体;
(2)硫酸钠和硝酸钡发生复分解反应生成硫酸钡沉淀和硝酸钠.
点评:本题考查学生离子方程式书写的知识,是现在高考的热点,难度不大.
(2)NaNO3溶液、Na2SO4溶液和NaCl溶液中,只有Na2SO4溶液和硝酸钡发生复分解反应生成白色沉淀,离子方程式是:SO42-+Ba2+=BaSO4↓,故答案为:SO42-+Ba2+=BaSO4↓.
分析:(1)硝酸和碳酸钠反应生成二氧化碳气体;
(2)硫酸钠和硝酸钡发生复分解反应生成硫酸钡沉淀和硝酸钠.
点评:本题考查学生离子方程式书写的知识,是现在高考的热点,难度不大.

练习册系列答案
相关题目
下列实验能达到预期目的是
| 编号 | 实验内容 | 实验目的 |
| A | 将SO2通入溴水,溴水褪色后加热观察能否恢复原色 | 验证SO2漂白的可逆性 |
| B | 将氯水加入淀粉KI溶液中 | 验证Cl的非金属性比I强 |
| C | 把铁块和铜块用导线连接插入浓硝酸中 | 组成原电池验证Fe比Cu活泼 |
| D | 加热氯化铵和碘单质的固体混合物 | 分离除去碘单质 |
- A.A
- B.B
- C.C
- D.D
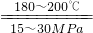 H2O+CO(NH2)2
H2O+CO(NH2)2