题目内容
对于已达平衡的可逆反应mA(g)+nB(g)
据图可知:
(1)该反应的正反应是____________(填“吸”或“放”)热反应。
(2)反应方程式中气体物质的化学计量数的关系是:m+n=___________p+q(填“>”“<”或“=”)。
(1)吸 (2)>
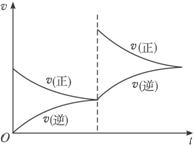
解析:由图分析,在同一压强不同温度下,升高温度时,A的转化率提高,表明化学平衡向正反应方向移动,则正反应为吸热反应;在同一温度不同压强下,增大压强时,A的转化率提高,表明化学平衡向正反应方向移动,则正反应为气体体积缩小的可逆反应,因此有m+n>p+q。

练习册系列答案
相关题目

 Fe(SCN)3,加入KCl固体,颜色不应该有变化,但现象却是变浅了,请你分析变浅的可能原因是_____________________。
Fe(SCN)3,加入KCl固体,颜色不应该有变化,但现象却是变浅了,请你分析变浅的可能原因是_____________________。