题目内容
【题目】某有机物X的结构简式如图所示,则下列有关说法中正确的是
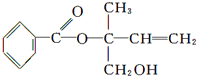
A. X的分子式为C12H16O3
B. 可用酸性高锰酸钾溶液区分苯和X
C. X在一定条件下能发生加成、加聚、取代、消去等反应
D. 在Ni作催化剂的条件下,1 mol X最多只能与1 mol H2加成
【答案】B
【解析】
试题A、根据有机物中碳原子的结构特点,此有机物的结构简式:C12H14O3,故错误;B、苯不能使酸性高锰酸钾褪色,而X中有羟基和碳碳双键,能使酸性高锰酸钾褪色,故正确;C、X中含有的官能团是酯基、羟基、碳碳双键,能发生加成、加聚、取代,羟基所连碳的相邻碳原子上无氢原子,不能发生消去反应,故错误;D、此有机物中能发生加成的反应的是苯环、碳碳双键,1mol苯环需要3mol氢气,1mol碳碳双键需要1mol氢气,因此1mol有机物最多与4mol氢气发生加成,故错误。

【题目】(2016·天津卷) 下表为元素周期表的一部分。
碳 | 氮 | Y | |
X | 硫 | Z |
回答下列问题:
(1)Z元素在周期表中的位置为__________。
(2)表中元素原子半径最大的是(写元素符号)__________。
(3)下列事实能说明Y元素的非金属性比S元素的非金属性强的是__________。
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1 mol Y单质比1 mol S得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(4)X与Z两元素的单质反应生成1 mol X的最高价化合物,恢复至室温,放热687 kJ,已知该化合物的熔、沸点分别为69 ℃和58 ℃,写出该反应的热化学方程式:__________。
(5)碳与镁形成的1 mol化合物Q与水反应,生成2 mol Mg(OH)2和1 mol烃,该烃分子中碳氢质量比为9∶1,烃的电子式为__________。Q与水反应的化学方程式为__________。
(6)铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,同时生成的两种气体均由上表中两种元素组成,气体的相对分子质量都小于50。为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗1 L 2.2 mol/L NaOH溶液和1 mol O2,则两种气体的分子式及物质的量分别为__________,生成硫酸铜物质的量为__________。