题目内容
(共6分)将100 mL 5 mol·L-1 NaOH(aq)稀释到500 mL ,稀释后溶液中NaOH的物质的量浓度为______________; 将氯气通入此溶液充分反应,可制得漂白液,漂白液的主要成分为_________________,其中有效成分为_________________ 。
(共6分) 1mol/L NaCl、NaClO NaClO

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
(本题共6分)
某学生课外兴趣小组为了测定镁铝合金中铝的含量,进行了如下实验。将合金3.0克投入到足量的100 mL 1.5 mol?L-1的烧碱溶液中,充分反应后分离出未反应的镁,然后在溶液中滴加1.0 mol?L-1的盐酸,加入盐酸的体积与得到沉淀的数据如下表:
| 实验次数 | 加入盐酸的体积 | 沉淀质量 |
| 1 | 60 mL | 0 |
| 2 | 80 mL | 0.78 g |
| 3 | 180 mL | 5.46 g |
(2)合金中铝的质量分数为 。
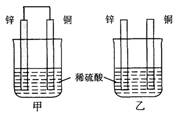
(本题共12分)将纯锌片和纯铜片按图方式插入100 mL相同浓度的稀硫酸中一段时间,回答下列问题:
(1)下列说法正确的是____________。
| A.甲、乙均为化学能转变为电能的装置 |
| B.乙中铜片上没有明显变化 |
| C.甲中铜片质量减少、乙中锌片质量减少 |
| D.两烧杯中溶液的c(H+)均增小 |
(3)当甲中产生1.12L(标准状况)气体时,通过导线的电子数目为_______________。
(4)当乙中产生1.12L(标准状况)气体时,将锌、铜片取出,再将烧杯中的溶液稀释至1 L,测得溶液中c(H+)=0.1 mol·L-1(设反应前后溶液体积不变)。试确定原稀硫酸的物质的量浓度为_________________。
(5) 甲中锌片上发生的电极反应: _________________________;
(6) 若甲中两电极的总质量为60 g,工作一段时间后,取出锌片和铜片洗净干燥后称重,总质量为47 g,则:氢气的体积(标准状况)为________。
(本题共6分)
某学生课外兴趣小组为了测定镁铝合金中铝的含量,进行了如下实验。将合金3.0克投入到足量的100 mL 1.5 mol•L-1的烧碱溶液中,充分反应后分离出未反应的镁,然后在溶液中滴加1.0 mol•L-1的盐酸,加入盐酸的体积与得到沉淀的数据如下表:
|
实验次数 |
加入盐酸的体积 |
沉淀质量 |
|
1 |
60 mL |
0 |
|
2 |
80 mL |
0.78 g |
|
3 |
180 mL |
5.46 g |
(1)开始沉淀时加入的盐酸体积必须大于 mL;若得到沉淀的量最大时,加入的盐酸体积为 mL。
(2)合金中铝的质量分数为 。