题目内容
A.B.C.为三种单质,B.C反应的产物溶于水得到的无色酸性溶液E,A.B反应的产物D溶于水得到黄色溶液,G为红褐色沉淀,各反应物之间的转化关系如图所示:
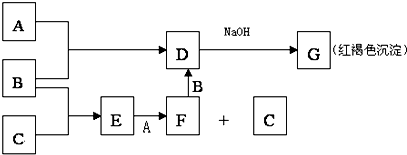
(1)A.B.C分别是 , , .(填化学式)
(2)写出B+F→D的化学方程式: .
(3)写出E+A→F+C的离子方程式: .
(4)写出D+NaOH→G的化学方程式: .

(1)A.B.C分别是
(2)写出B+F→D的化学方程式:
(3)写出E+A→F+C的离子方程式:
(4)写出D+NaOH→G的化学方程式:
考点:无机物的推断
专题:推断题
分析:A、B、C为三种单质,A、B反应的产物D溶于水得到黄色溶液,D与氢氧化钠反应得到G为红褐色沉淀,则G为Fe(OH)3,故D为FeCl3,而B、C反应的产物溶于水得到的无色酸性溶液E,故A为Fe、B为Cl2,C为H2,E为HCl,结合转化关系可知,F为FeCl2,据此解答.
解答:
解:A、B、C为三种单质,A、B反应的产物D溶于水得到黄色溶液,D与氢氧化钠反应得到G为红褐色沉淀,则G为Fe(OH)3,故D为FeCl3,而B、C反应的产物溶于水得到的无色酸性溶液E,故A为Fe、B为Cl2,C为H2,E为HCl,结合转化关系可知,F为FeCl2,
(1)由上述分析可知,A、B、C分别是:Fe,Cl2,H2,故答案为:Fe;Cl2;H2;
(2)B+F→D的化学方程式:2FeCl2+Cl2=2FeCl3,故答案为:2FeCl2+Cl2=2FeCl3;
(3)E+A→F+C的离子方程式:Fe+2H+=Fe2++H2↑,故答案为:Fe+2H+=Fe2++H2↑;
(4)D+NaOH→G的化学方程式:FeCl3+3NaOH=Fe(OH)3↓+3NaCl,故答案为:FeCl3+3NaOH=Fe(OH)3↓+3NaCl.
(1)由上述分析可知,A、B、C分别是:Fe,Cl2,H2,故答案为:Fe;Cl2;H2;
(2)B+F→D的化学方程式:2FeCl2+Cl2=2FeCl3,故答案为:2FeCl2+Cl2=2FeCl3;
(3)E+A→F+C的离子方程式:Fe+2H+=Fe2++H2↑,故答案为:Fe+2H+=Fe2++H2↑;
(4)D+NaOH→G的化学方程式:FeCl3+3NaOH=Fe(OH)3↓+3NaCl,故答案为:FeCl3+3NaOH=Fe(OH)3↓+3NaCl.
点评:本题考查无机物推断,难度不大,物质的颜色是推断突破口,结合转化关系推断,需要学生熟练掌握元素化合物性质.

练习册系列答案
相关题目
用来检验酒精中是否含有水的试剂是( )
| A、碱石灰 |
| B、CuSO4 |
| C、浓硫酸 |
| D、金属钠 |
50mL 0.3mol/L的AlCl3溶液加水稀释到500mL,稀释后溶液中Cl-的物质的量浓度为( )
| A、0.03mol/L |
| B、0.09mol/L |
| C、0.045mol/L |
| D、0.015mol/L |

 .
.

