题目内容
由两种烃组成的混合气体2L与足量的氧气充分反应后生成CO2 5L,H2O 7L(所有体积都在120℃测定),则这两种混合气体的可能组成是( )
分析:同温同压下,气体的体积之比等于物质的量之比,可得混合气体的最简式为C2.5H7,根据C原子可计算混合气体的物质的量之比,然后根据所求得的物质的量之比计算H原子数是否为7,以此解答.
解答:解:同温同压下,气体的体积之比等于物质的量之比,可得混合气体的最简式为C2.5H7,
A、当C=2.5时,两种烃的物质的量之比为1:1,含H原子数为6,不符合,故A错误;
B、当C=2.5时,两种烃的物质的量之比为5:3,含H原子数为5.5,不符合,故B错误;
C、当C=2.5时,两种烃的物质的量之比为1:1,含H原子数为6,不符合,故C错误;
D、当C=2.5时,两种烃的物质的量之比为1:1,含H原子数为7,符合,故D正确.
故选D.
A、当C=2.5时,两种烃的物质的量之比为1:1,含H原子数为6,不符合,故A错误;
B、当C=2.5时,两种烃的物质的量之比为5:3,含H原子数为5.5,不符合,故B错误;
C、当C=2.5时,两种烃的物质的量之比为1:1,含H原子数为6,不符合,故C错误;
D、当C=2.5时,两种烃的物质的量之比为1:1,含H原子数为7,符合,故D正确.
故选D.
点评:本题考查混合物的计算,题目难度中等,本意不能直接用最简式排除,应根据C的平均原子数计算H的平均原子数进行排除计算.

练习册系列答案
 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
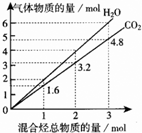 两种气态烃组成的混合气体完全燃烧后所得到CO2和H2O的物质的量随混合烃总物质的量的变化如图所示.下列有关混合气体的说法正确的是( )
两种气态烃组成的混合气体完全燃烧后所得到CO2和H2O的物质的量随混合烃总物质的量的变化如图所示.下列有关混合气体的说法正确的是( ) 成;
成;