题目内容
已知反应:
①25℃、101kP a时:N2H4(g)+O2(g)=N2(g)+2H2O(g);△H =-534 kJ·mol-1
a时:N2H4(g)+O2(g)=N2(g)+2H2O(g);△H =-534 kJ·mol-1
②稀溶液中:H+(aq)+OH-(aq)=H2O(l);△H=-57.3 kJ·mol-1
下列结论正确的是 ( )
①25℃、101kP
 a时:N2H4(g)+O2(g)=N2(g)+2H2O(g);△H =-534 kJ·mol-1
a时:N2H4(g)+O2(g)=N2(g)+2H2O(g);△H =-534 kJ·mol-1②稀溶液中:H+(aq)+OH-(aq)=H2O(l);△H=-57.3 kJ·mol-1
下列结论正确的是 ( )
| A.N2H4的燃烧热大于534 kJ·mol-1 |
| B.①的反应热为221 kJ·mol-1 |
| C.稀硫酸与稀NaOH溶液反应的中和热为-57.3 kJ·mol-1 |
| D.稀醋酸与稀NaOH溶液反应生成l mol水,放出57.3 kJ热量 |
A
1 mol N2H4在101 kPa 25℃时完全燃烧生成N2和液态水所放出的热量叫N2H4的燃烧热,现1 mol N2H4完全燃烧生成气态水放热534 kJ,易知N2H4的燃烧热大于534 kJ·mol-1,反应①的反应热△H =-534 kJ·mol-1,A对B错;稀H2SO4与稀NaOH溶液反应的中和热为57.3 kJ·mol-1不必加“-”,C错;CH3COOH是弱酸,其电离是吸热反应,故与NaOH溶液中和生成1 mol H2O时放出热量小于57.3 kJ。

练习册系列答案
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案
相关题目
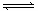 H++OH— △H>0,下列叙述正确的是( )
H++OH— △H>0,下列叙述正确的是( )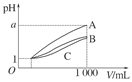
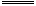 H2O(l);△H="-57.4" kJ/mol
H2O(l);△H="-57.4" kJ/mol  2H2(g)+O2(g);△H=" +483.6" kJ· mol—1,则氢气的燃烧热为241.8kJ/mol
2H2(g)+O2(g);△H=" +483.6" kJ· mol—1,则氢气的燃烧热为241.8kJ/mol ________25 ℃。
________25 ℃。