题目内容
下列说法或表示方法正确的是( )
| A.若将等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| B.由“C(石墨)=C(金刚石) ΔH=1.9 kJ·mol” 可知,金刚石比石墨稳定 |
| C.在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l) ΔH=-285.8 kJ/mol |
| D.在稀溶液中:H++OH-=H2O ΔH=-57.3 kJ·mol ,若将含1 mol H2SO4与含2 mol NaOH的溶液混合,放出的热量等于114.6 kJ |
D
S(g)转化成S(s)需要放出热量,因此燃烧等量的硫蒸气放出的热量多于硫固体,A错;由石墨转变为金刚石需吸收热量,说明石墨的能量低于金刚石,石墨比金刚石稳定,B错;2 mol H2的质量为4 g,因此ΔH=-571.6 kJ/mol,C错;1 mol H2SO4与2 mol NaOH反应生成2 mol H2O,放出的热量等于114.6 kJ,D对。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 NH3↑+HCl↑
NH3↑+HCl↑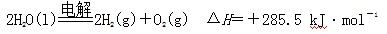
 NH3↑+HCl↑
NH3↑+HCl↑ NH4HCO3
NH4HCO3