题目内容
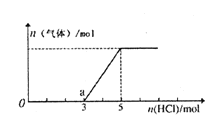
【题目】将一定量的CO2气体通入2L的NaOH溶液中,在所得溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的气体与消耗的HC1物质的量关系如图所示(忽略气体的溶解和HC1的挥发).下列说法不正确的是
A. 0点溶液中所含溶质的化学式为NaOH、Na2CO3
B. 0到a点发生反应的离子方程式:H++OH-=H2O、CO32-+H+=HCO3-
C. 通入CO2气体的体积在标准状况下为22.4L
D. NaOH溶液的物质的量浓度为2.5mol/L
【答案】C
【解析】A、Na2CO3跟盐酸的反应是分步进行的:Na2CO3+HCl=NaHCO3+NaCl,NaHCO3+HCl=NaCl+H2O+CO2↑,HCl与Na2CO3、NaHCO3都按1:1反应,由图象可知生成二氧化碳消耗的HCl的物质的量小于从反应到开始产生二氧化碳阶段消耗的HCl,故溶液中溶质为NaOH、Na2CO3,选项A正确;B、根据A分析可知,0到a点发生反应为:氢离子与氢氧根离子反应生成水,氢离子与碳酸根反应生成碳酸氢根,发生的离子反应为:H++OH-=H2O、CO32-+H+=HCO3-,选项B正确;C、由图可知,a点时开始生成气体,故发生反应为:NaHCO3+HCl=NaCl+H2O+CO2↑,至生成二氧化碳体积最大时,该阶段消耗的HCl的物质的量为2mol,由方程式可知产生二氧化碳的物质的量为2mol,生成的二氧化碳的物质的量等于开始通入的二氧化碳的物质的量,故开始通入的二氧化碳的体积为2mol×22.4L/mol=44.8L,选项C不正确;D、加入5molNaCL生成二氧化碳体积最大,此时溶液中溶质为NaCl,根据氯离子守恒有n(NaCl)=n(HCl),根据钠离子守恒有n(NaOH)=n(NaCl),故n(NaOH)=n(HCl)=5mL,所以c(NaOH)=![]() =2.5mol/L,选项D正确。答案选C。
=2.5mol/L,选项D正确。答案选C。

【题目】下表中金属的冶炼原理与方法不完全正确的是( )
选项 | 冶炼原理 | 方法 |
A | 2HgO=2Hg+O2 | 热分解法 |
B | 2Al2O3 (熔融)=4Al+3O2 | 电解法 |
C | Cu2S+O2=2Cu+SO2 | 热分解法 |
D | Fe2O3 +2Al=2Fe+Al2O3 | 热还原法 |
A. AB. BC. CD. D