题目内容
(9分)实验室可用NaBr、浓H2SO4、乙醇为原料制备少量溴乙烷:
C2H5—OH+HBr C2H5Br+H2O
C2H5Br+H2O
已知反应物的用量为:0.30 mol NaBr(s);0.25 mol C2H5OH(密度为0.80 g·cm-3);36 mL浓H2SO4(质量分数为98%,密度为1.84 g·mL-1);25 mL水。试回答下列问题。
(1)该实验应选择图中的a装置还是b装置?_____________。

(2)反应装置中的烧瓶应选择下列哪种规格最合适( )
A.50 mL B.100 mL C.150 mL D.250 mL
(3)冷凝管中的冷凝水的流向应是 ( )
A. A进B出 B. B进A出 C. 从A进或B进均可
(4)可能发生的副反应为:_____________、__________、______________(至少写出3个方程式)。
(5)实验完成后,须将烧瓶内的有机物蒸出,结果得到棕黄色的粗溴乙烷,欲得纯净溴乙烷,应采用的措施是_______ _________。
(1)a。(1分) (2)C (1分) (3)B (1分)
(4)C2H5OH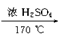 C2H4↑+H2O
C2H4↑+H2O
2C2H5OH
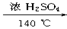 C2H5OC2H5+H2O(3分)
C2H5OC2H5+H2O(3分)
2HBr+H2SO4(浓) Br2+SO2↑+2H2O
Br2+SO2↑+2H2O
C2H5OH+2H2SO4(浓)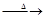 2C+2SO2↑+5H2O
2C+2SO2↑+5H2O
C+2H2SO4(浓) CO2↑+2SO2↑+2H2O(任意选取3个反应即可)(3分)
CO2↑+2SO2↑+2H2O(任意选取3个反应即可)(3分)
(5)加入NaOH溶液后,分液,再把产品水洗,蒸馏即可。
【解析】
(1)由于需要加热,所以应选a装置
(2)乙醇体积=0.25*46/0.80(mL)=14.375mL,溶液总体积=36ml+25ml+14mL=75mL,加热时溶液体积不能超过选用容器体积的一半,接近一半最好,故选用150mL烧瓶
(5)棕黄色的粗溴乙烷含有很多的无机试剂H2SO4、NaBr、NaHSO4等,将粗溴乙烷和稀NaOH(aq)的混合物放在分液漏斗中用力振荡,并不断放气,至油层无色,分液可得纯溴乙烷

 优生乐园系列答案
优生乐园系列答案 实验室可用NaBr、浓H2SO4、乙醇为原料制备少量溴乙烷:
实验室可用NaBr、浓H2SO4、乙醇为原料制备少量溴乙烷:

 C2H5Br+H2O
C2H5Br+H2O