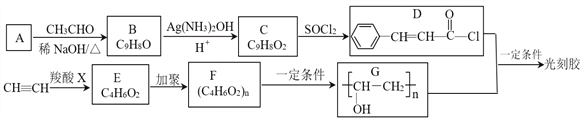
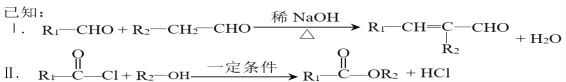
题目内容
【题目】0.01molL﹣1的某一元弱酸溶液 pH=4,则它的电离度为( )
A.1%
B.2%
C.5%
D.10%
【答案】A
【解析】解:设此一元弱酸为HX,则电离方程式为:HX=H++X﹣ , 设其电离度为α,则电离的弱酸浓度为0.01α,
溶液pH=4,则电离出的[H+]=10﹣4 , 即0.01α=10﹣4 , 故α=1%.
故选A.
根据弱电解质的电离平衡方程式,利用pH和氢离子浓度之间的关系来计算.

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案
相关题目