题目内容
洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。根据所学知识,回答下列问题:
(1)工业上将氯气通入石灰乳制取漂白粉,化学反应方程式为____________________。
(2)漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学反应方程式为 _______ ____________________________ 。
____________________________ 。
(3)制取漂白粉的氯气可通过电解饱和食盐水得到。在电解食盐水之前,需要提纯食盐水。为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列五项操作,正确的操作顺序是 。
①过滤 ②加过量的NaOH溶液 ③加适量的盐酸
④加过量的Na2CO3溶液 ⑤加过量的BaCl2溶液
(4) 极滴入酚酞先变红色(填阴或阳),石墨棒的一端能使湿润的淀粉碘化钾试纸 。
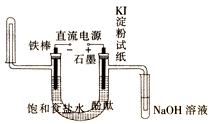
(5)假如电解饱和食盐水制取氯气,氯气制取漂白粉过程中没有任何损耗,得到715 g次氯酸钙的同时,理论上需要消耗NaCl的物质的量为多少? (4分)
g次氯酸钙的同时,理论上需要消耗NaCl的物质的量为多少? (4分)
(1)工业上将氯气通入石灰乳制取漂白粉,化学反应方程式为____________________。
(2)漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学反应方程式为 _______
 ____________________________ 。
____________________________ 。(3)制取漂白粉的氯气可通过电解饱和食盐水得到。在电解食盐水之前,需要提纯食盐水。为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列五项操作,正确的操作顺序是 。
①过滤 ②加过量的NaOH溶液 ③加适量的盐酸
④加过量的Na2CO3溶液 ⑤加过量的BaCl2溶液
| A.①④②⑤③ | B.④①②⑤③ | C.②⑤④①③ | D.⑤②④③① |

(5)假如电解饱和食盐水制取氯气,氯气制取漂白粉过程中没有任何损耗,得到715
 g次氯酸钙的同时,理论上需要消耗NaCl的物质的量为多少? (4分)
g次氯酸钙的同时,理论上需要消耗NaCl的物质的量为多少? (4分)(14分)
(1)2Cl2+2Ca(OH)2 = CaCl2+Ca(ClO)2+2H2O
(2) Ca(ClO)2+CO2+H2O ==CaCO3↓+2HClO
(3)C (4)阴 变蓝(5)20 mol(4分)
(1)2Cl2+2Ca(OH)2 = CaCl2+Ca(ClO)2+2H2O
(2) Ca(ClO)2+CO2+H2O ==CaCO3↓+2HClO
(3)C (4)阴 变蓝(5)20 mol(4分)
略

练习册系列答案
相关题目
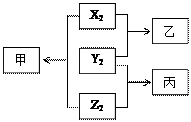
 。
。
 O2作用下,先用NaClO将CN-离子氧化成CNO-,再在酸性条件下继续被NaClO氧化成N2和CO2。环保工作人员在密闭系统中
O2作用下,先用NaClO将CN-离子氧化成CNO-,再在酸性条件下继续被NaClO氧化成N2和CO2。环保工作人员在密闭系统中 用下图装置进行实验,以证明处理方法的有效性,并测定CN-被处理的百分率。
用下图装置进行实验,以证明处理方法的有效性,并测定CN-被处理的百分率。
 液全部放入乙中,关闭活塞。回答下列问题:
液全部放入乙中,关闭活塞。回答下列问题: 成的气体除N2和CO2外,还有HCl及副产物Cl2等,上述实验是通过测定二氧化碳的量来确定对CN-的处理效果。则丙中加入的除杂试剂是__ __(填字母)
成的气体除N2和CO2外,还有HCl及副产物Cl2等,上述实验是通过测定二氧化碳的量来确定对CN-的处理效果。则丙中加入的除杂试剂是__ __(填字母)
 验中戊中共生成0.82 g沉淀,则该实验中测得CN-被处理的百分率等于___ _____,请说明该测得值与实际处理的百分率相比偏高还是偏低_ ___?简要说明可能的原因________________________ _________ _________。
验中戊中共生成0.82 g沉淀,则该实验中测得CN-被处理的百分率等于___ _____,请说明该测得值与实际处理的百分率相比偏高还是偏低_ ___?简要说明可能的原因________________________ _________ _________。