题目内容
【题目】下列过程中,共价键被破坏的是( )
A.碘升华
B.溴蒸气被木炭吸附
C.蔗糖溶于水
D.SO2气体溶于水
【答案】D
【解析】解:A.碘升华克服的是分子间作用力,共价键没有破坏,故A错误; B.溴蒸气被木炭吸附,没有发生化学变化,也没有电离,所以共价键没有破坏,故B错误;
C.蔗糖属于非电解质,溶于水,不发生电离,也不反应,共价键没有破坏,故C错误;
D.SO2气体溶于水,与水发生了化学反应,共价键被破坏,故D正确.
故选D.

 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案【题目】在无色溶液中大量共存的一组离子是
A. Cu2+、SO42-、K+、Cl- B. Ag+、Cl-、OH-、Na+
C. NO3-、Cl-、Na+、Ca2+ D. NO3-、OH-、Mg2+、Na+
【题目】下表是某学生为探究AgCl沉淀转化为Ag2S沉淀的反应所做实验的记录.
步 骤 | 现 象 |
Ⅰ.取5mL 0.1mol/L AgNO3与一定体积0.1mol/L NaCl溶液,混合,振荡. | 立即产生白色沉淀 |
Ⅱ.向所得悬浊液中加入2.5mL 0.1mol/L Na2S溶液. | 沉淀迅速变为黑色 |
Ⅲ.将上述黑色浊液,放置在空气中,不断搅拌. | 较长时间后,沉淀变为乳白色 |
Ⅳ.滤出Ⅲ中的乳白色沉淀,加入足量HNO3溶液. | 产生红棕色气体,沉淀部分溶解 |
Ⅴ.过滤得到滤液X和白色沉淀Y;向X中滴加Ba(NO3)2溶液. | 产生白色沉淀 |
(1)为了证明沉淀变黑是AgCl转化为Ag2S的缘故,步骤I中NaCl溶液的体积范围为 .
(2)已知:25℃时Ksp(AgCl)=1.8×10﹣10 , Ksp(Ag2S)=6×10﹣30 , 此沉淀转化反应的平衡常数K .
(3)步骤V中产生的白色沉淀的化学式为 , 步骤Ⅲ中乳白色沉淀除含有AgCl外,还含有 .
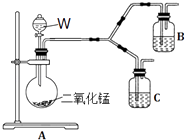
(4)为了进一步确认步骤Ⅲ中乳白色沉淀产生的原因,设计了如下图所示的对比实验装置. ①装置A中玻璃仪器有圆底烧瓶、导管和 , 试剂W为 .
②装置C中的试剂为NaCl溶液和Ag2S悬浊液的混合物,B中试剂为 .
③实验表明:C中沉淀逐渐变为乳白色,B中没有明显变化.
完成C中反应的化学方程式:
Ag2S+NaCl++AgCl+S+
C中NaCl的作用是: