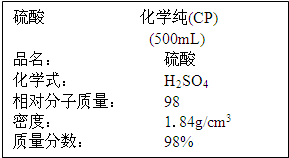
题目内容
已知实验室中有一瓶失去标签的AgNO3溶液,取出其100mL溶液于烧杯之中,加入足量上述实验题中所配制的NaCl溶液,经反应完毕后,过滤、洗涤、干燥得到28.7克沉淀.已知AgNO3溶液的密度为ρ=1.13g?mL-1
回答下列问题:
(1)洗涤AgCl沉淀的操作?
(2)则该AgNO3溶液的物质的量浓度是多少?质量分数是多少?.
回答下列问题:
(1)洗涤AgCl沉淀的操作?
(2)则该AgNO3溶液的物质的量浓度是多少?质量分数是多少?.
(1)洗涤AgCl沉淀的操作为:向过滤器中注入蒸馏水,使水浸没沉淀物,当水滤完后重复操作数次,
答:洗涤AgCl沉淀应向过滤器中注入蒸馏水,使水浸没沉淀物,当水滤完后重复操作数次;
(2)28.7g为AgCl的质量,其物质的量=
=0.2mol,根据Ag元素守恒可知n(AgNO3)=n(AgCl)=0.2mol,故AgNO3的物质的量浓度=
=2mol/L;
根据c=
可知,硝酸银溶液的质量分数=
=30%,
答:该AgNO3溶液的物质的量浓度是2mol/L,质量分数是30%.
答:洗涤AgCl沉淀应向过滤器中注入蒸馏水,使水浸没沉淀物,当水滤完后重复操作数次;
(2)28.7g为AgCl的质量,其物质的量=
| 28.7g |
| 143.5g/mol |
| 0.2mol |
| 0.1L |
根据c=
| 1000ρw |
| M |
| 2×170 |
| 1000×1.13 |
答:该AgNO3溶液的物质的量浓度是2mol/L,质量分数是30%.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目