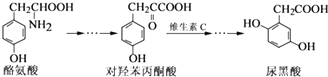
��Ŀ����
����Ŀ����һ�������Ba(OH)2��Һ����OH-�����ʵ���Ũ��Ϊ0.01mol/L����������μ���һ�����ʵ���Ũ�ȵ�NaHSO4��Һ������Һ�е�Ba2+ǡ����ȫ����ʱ����Һ��OH-�����ʵ���Ũ��Ϊ0.001mol/L��
��1����Ba(OH)2��Һ��Ba(OH)2�����ʵ���Ũ��Ϊ__________________��
��2��Ba2+ǡ����ȫ����ʱ��������Ӧ�����ӷ���ʽΪ_______________________��
��3������Ӧ����Һ���������Ba(OH)2��NaHSO4��Һ�����֮�ͣ���Ba(OH)2��Һ��NaHSO4��Һ���������__________��
��4������NaHSO4��Һ������Ba(OH)2��Һ�����ԣ�������Ӧ�����ӷ���ʽΪ__________________________��
���𰸡� 0.005mol/L Ba2++OH-+H++SO42-=BaSO4��+H2O 1:4 Ba2++SO42-+2H++2OH-=BaSO4��+2H2O��
����������һ�������Ba(OH)2��Һ�У�OH-�����ʵ���Ũ��Ϊ0.01mol/L����������μ���һ�����ʵ���Ũ�ȵ�NaHSO4��Һ������Һ�е�Ba2+ǡ����ȫ����ʱ����Һ��OH-�����ʵ���Ũ��Ϊ0.001mol/L��
��1��Ba(OH)2��Һ��OH-�����ʵ���Ũ��Ϊ0.01mol/L�����ݻ�ѧʽ��֪Ba(OH)2�����ʵ���Ũ��Ϊ0.01mol/L��2��0.005mol/L����2��Ba2+ǡ����ȫ����ʱ�������ᱵ���������ƺ�ˮ��������Ӧ�����ӷ���ʽΪBa2++OH-+H++SO42-=BaSO4��+H2O����3����Ba(OH)2��Һ��NaHSO4��Һ������ֱ���xL��yL�����ݷ���ʽ��֪���������е�������ǡ�÷�Ӧһ�룬��![]() �����x��y��1��4����4����NaHSO4��Һ������Ba(OH)2��Һ������ʱ�������ᱵ�������ƺ�ˮ��������Ӧ�����ӷ���ʽΪBa2++SO42-+2H++2OH-=BaSO4��+2H2O��
�����x��y��1��4����4����NaHSO4��Һ������Ba(OH)2��Һ������ʱ�������ᱵ�������ƺ�ˮ��������Ӧ�����ӷ���ʽΪBa2++SO42-+2H++2OH-=BaSO4��+2H2O��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�