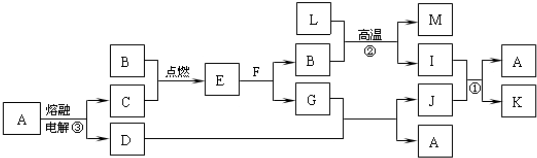
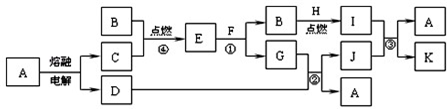
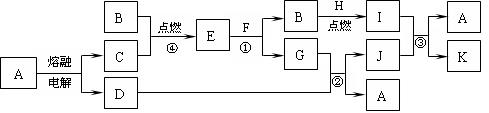
题目内容
| |||||||||||
答案:
解析:
解析:
(1) |
淀粉溶液,蓝色刚好褪去 |
(2) |
由①②方程式可知:IO3-~3I2~6S2O32- n(IO3-)= 则250g样品中含有碘元素的质量为:2×10-5mol×127g/mol×1000mg/g=2.54mg该加碘食盐中碘元素的含量为: 因为10.16mg/kg<20mg/kg,所以该加碘盐不合格 |

练习册系列答案
 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案
相关题目