题目内容
下列变化或数据与氢键无关的是( )
| A、甲酸蒸气的密度在373K时为1.335g?L-1,在293K时为2.5g?L-1 |
| B、氨分子与水分子形成一水合氨 |
| C、水结冰体积增大 |
| D、SbH3的沸点比PH3高 |
考点:含有氢键的物质
专题:化学键与晶体结构
分析:A.373K时,甲酸蒸气中分子距离较大,不形成氢键;293K时,甲酸为液体,存在氢键;
B.一水合氨分子是氨分子中的氢原子和水分子中的氧原子之间通过氢键形成的;
C.冰中的氢键比液态水中的强,使得水分子排列得很规则,造成体积膨胀,密度变小;
D.分子晶体,相对分子质量越大,沸点越高.
B.一水合氨分子是氨分子中的氢原子和水分子中的氧原子之间通过氢键形成的;
C.冰中的氢键比液态水中的强,使得水分子排列得很规则,造成体积膨胀,密度变小;
D.分子晶体,相对分子质量越大,沸点越高.
解答:
解:A.373K时,甲酸蒸气中分子距离较大,不形成氢键;293K时,甲酸为液体,存在氢键,故A不选;
B.一水合氨分子是氨分子中的氢原子和水分子中的氧原子之间通过氢键形成的,故B不选;
C.冰中的氢键比液态水中的强,使得水分子排列得很规则,造成体积膨胀,密度变小,故C不选;
D.SbH3和PH3都是分子晶体,相对分子质量越大,沸点越高,故SbH3的沸点比PH3高,与氢键无关,故D选,
故选D.
B.一水合氨分子是氨分子中的氢原子和水分子中的氧原子之间通过氢键形成的,故B不选;
C.冰中的氢键比液态水中的强,使得水分子排列得很规则,造成体积膨胀,密度变小,故C不选;
D.SbH3和PH3都是分子晶体,相对分子质量越大,沸点越高,故SbH3的沸点比PH3高,与氢键无关,故D选,
故选D.
点评:本题考查氢键对物质性质的影响,难度不大.要注意氢键只影响物质的物理性质.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列气态氢化物最稳定的是( )
| A、HF |
| B、HCl |
| C、HBr |
| D、H2S |
维生素C的结构简式为: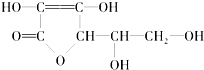
丁香油酚的结构简式为: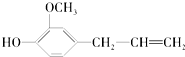
下列关于二者所含官能团的说法正确的是( )

丁香油酚的结构简式为:

下列关于二者所含官能团的说法正确的是( )
| A、均含酯基 |
| B、均含醇羟基和酚羟基 |
| C、均含碳碳双键 |
| D、均为芳香族化合物 |
下列图示与对应的叙述正确的是( )
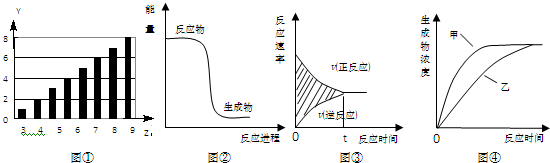

| A、图①所示柱形图,纵坐标表示第二周期元素最高正价随原子序数的变化 |
| B、图②所示曲线,表示该反应是吸热反应 |
| C、图③所示曲线的阴影部分面积,表示正反应速率改变值 |
| D、图④所示曲线,甲、乙分别表示有、无催化剂时发生的反应 |
在下列溶液中,一定能大量共存的离子组是( )
A、常温下
| ||
| B、含有大量Al3+的溶液中:SO42-、S2-、AlO2-、ClO- | ||
| C、能使pH试纸显蓝色的溶液中:K+、Ba2+、Cl-、Br- | ||
| D、常温下,在由水电离出的c(H+)=1×10-13mol?L-1的溶液中:K+、Fe3+、Cl-、SO42- |
分子式为C5H11OH的醇同分异构体共有(不考虑立体异构)( )
| A、6种 | B、7种 | C、8种 | D、9种 |
下列物质中,属于混合物的是( )
| A、碳酸钠 | B、液态氨 |
| C、铝热剂 | D、氢氧化钠 |
在下列溶液中,能大量共存的一组离子是( )
| A、pH=1的溶液中:NH4+、Fe2+、SO42-、ClO- |
| B、通入过量SO2气体的溶液中:Fe3+、NO3-、Ba2+、H+ |
| C、c(Al3+)=0.1mol/L的溶液中:Na+、K+、AlO2-、SO42- |
| D、通入过量CO2气体的溶液中:Na+、Ba2+、HCO3-、Cl-、Br- |
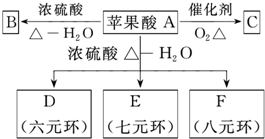 苹果醋(ACV)是一种由苹果发酵而成的酸性饮品,具有解毒、降脂等药效,主要酸性物质为苹果酸.该苹果酸在分离提纯后的化学分析如下:
苹果醋(ACV)是一种由苹果发酵而成的酸性饮品,具有解毒、降脂等药效,主要酸性物质为苹果酸.该苹果酸在分离提纯后的化学分析如下: