题目内容
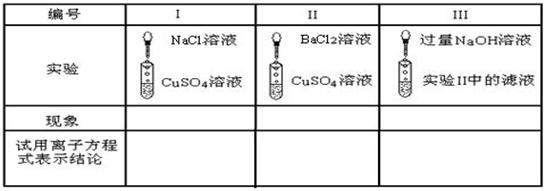
以下表格中的实验是以CuSO4为例,分析电解质在溶液里所起反应的实质:| 编号 | Ⅰ | Ⅱ | Ⅲ |
| 实验 |  NaCl溶液 NaCl溶液CuSO4溶液 |
 BaCl2溶液 BaCl2溶液CuSO4溶液 |
 过量NaOH 溶液 过量NaOH 溶液实验Ⅱ中的溶液 |
| 现象 | |||
| 试用离子方程式表示结论 |
分析:Ⅰ.氯化钠溶液与硫酸铜溶液混合后,不满足离子反应发生条件,二者不会反应,没有明显现象;
Ⅱ.氯化钡加入硫酸铜溶液中,氯化钡与硫酸铜反应生成白色硫酸钡沉淀;
Ⅲ.氢氧化钠与铜离子反应生成蓝色的氢氧化铜沉淀.
Ⅱ.氯化钡加入硫酸铜溶液中,氯化钡与硫酸铜反应生成白色硫酸钡沉淀;
Ⅲ.氢氧化钠与铜离子反应生成蓝色的氢氧化铜沉淀.
解答:解:Ⅰ.氯化钠溶液滴入硫酸铜溶液中,氯化钠与硫酸铜之间不满足离子反应发生条件,所以二者不反应,
故答案为:无明显现象;无;
Ⅱ.氯化钡溶液滴入硫酸铜溶液中,钡离子与硫酸根离子反应生成白色沉淀硫酸钡,反应的离子方程式为Ba2++SO42-═BaSO4↓,
故答案为:产生白色沉淀;Ba2++SO42-═BaSO4↓;
Ⅲ.氢氧化钠溶液滴入实验Ⅱ中的溶液,氢氧根离子与铜离子反应生成蓝色的氢氧化铜沉淀,反应的离子方程式为Cu2++2OH-═Cu(OH)2↓,
故答案为:产生蓝色沉淀;Cu2++2OH-═Cu(OH)2↓.
故答案为:无明显现象;无;
Ⅱ.氯化钡溶液滴入硫酸铜溶液中,钡离子与硫酸根离子反应生成白色沉淀硫酸钡,反应的离子方程式为Ba2++SO42-═BaSO4↓,
故答案为:产生白色沉淀;Ba2++SO42-═BaSO4↓;
Ⅲ.氢氧化钠溶液滴入实验Ⅱ中的溶液,氢氧根离子与铜离子反应生成蓝色的氢氧化铜沉淀,反应的离子方程式为Cu2++2OH-═Cu(OH)2↓,
故答案为:产生蓝色沉淀;Cu2++2OH-═Cu(OH)2↓.
点评:本题考查了离子反应发生条件、离子方程式的书写,题目难度不中等,注意掌握离子反应发生条件及离子方程式的书写方法,试题培养了学生灵活应用所学知识的能力.

练习册系列答案
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案
相关题目