题目内容
(12分)2009年2月3日下午,山西省太原市第四人民医院举行了祝贺太原禽流感患儿彭杰(女)康复出院及病情报告会。禽流感病毒是一种没有超常抵抗力的病毒。研究证明,许多常用消毒药品如漂粉精、漂白粉、高锰酸钾等,都可以将禽流感病毒杀灭。氯气及氢氧化钙充分反应,使次氯酸钙成为主要成分,得到漂粉精,其稳定性比漂白粉高。
将漂粉精溶于适量水中,呈白色浊状物,静置沉降。取少许上层清液,滴加碳酸钠溶液出现白色沉淀,发生反应的离子方程式为______________________________。另取少许上层清液,先滴加适量的________(填化学式)酸化,再滴加________(填化学式)溶液即可检验Cl-的存在,发生反应的离子方程式为____________________________。再取少许上层清液,滴加几滴酚酞溶液,溶液呈红色,随后溶液迅速褪色,说明漂粉精溶液呈______性并具有______性。
将漂粉精溶于适量水中,呈白色浊状物,静置沉降。取少许上层清液,滴加碳酸钠溶液出现白色沉淀,发生反应的离子方程式为______________________________。另取少许上层清液,先滴加适量的________(填化学式)酸化,再滴加________(填化学式)溶液即可检验Cl-的存在,发生反应的离子方程式为____________________________。再取少许上层清液,滴加几滴酚酞溶液,溶液呈红色,随后溶液迅速褪色,说明漂粉精溶液呈______性并具有______性。
Ca2++CO===CaCO3↓ 稀硝酸
AgNO3 Ag++Cl-===AgCl↓ 碱 漂白
AgNO3 Ag++Cl-===AgCl↓ 碱 漂白
氯气与氢氧化钙充分发生反应:2Cl2+2Ca(OH)2===CaCl2+Ca(ClO)2+2H2O,使次氯酸钙成为主要成分,得到漂粉精,将漂粉精溶于水中,水变浑浊并有少量沉淀,取上层清液其主要成分是CaCl2、Ca(ClO)2,遇Na2CO3溶液,发生的反应可用离子方程式Ca2++CO===CaCO3↓表示,取上层清液滴加适量HNO3酸化排除杂质离子的干扰,再滴加AgNO3溶液,若出现白色沉淀,可证明有Cl-的存在,发生反应的离子方程式为:Ag++Cl-===AgCl↓,由于上层清液滴加几滴酚酞溶液,溶液呈红色,说明漂粉精溶液呈碱性,随后溶液迅速褪色,说明其溶液还具有漂白性。

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
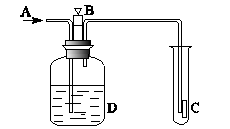
 NH3↑+HCl↑,推测:NH4I
NH3↑+HCl↑,推测:NH4I