题目内容
用石墨为电极材料电解时,下列说法正确的是( )
| A、电解NaOH溶液时,溶液浓度将减小,pH不变 |
| B、电解H2SO4溶液时,溶液浓度将增大,pH不变 |
| C、电解Na2SO4溶液时,溶液浓度将增大,pH不变 |
| D、电解NaCl溶液时,溶液浓度将减小,pH不变 |
考点:电解原理
专题:电化学专题
分析:以石墨为电极电解含氧酸、强碱、氢之前金属的含氧酸盐溶液时,实质上是电解水,如果用石墨电解氢之前金属的氯化物溶液时,阳极上氯离子放电,根据溶液中氢离子或氢氧根离子浓度是否变化确定溶液pH是否变化,据此分析解答.
解答:
解:A.用石墨作电极电解NaOH溶液时,阳极上氢氧根离子放电、阴极上氢离子放电,所以实质上是电解水,NaOH的物质的量不变,溶液体积减小,则溶液中NaOH增大,pH变大,故A错误;
B.用石墨作电极电解H2SO4溶液时,阳极上氢氧根离子放电、阴极上氢离子放电,所以实质上是电解水,硫酸的物质的量不变,溶液体积减小,则溶液中硫酸浓度增大,溶液的pH减小,故B错误;
C.用石墨电极电解硫酸钠溶液时,阳极上氢氧根离子放电、阴极上氢离子放电,所以实质上是电解水,硫酸钠的物质的量不变,溶液体积减小,硫酸钠的浓度增大,但硫酸钠溶液呈中性,所以溶液的PH不变,故C正确;
D.用石墨作电极电解NaCl溶液时,阳极上氯离子放电、阴极上氢离子放电,导致溶液中有氢氧根离子生成,则溶液中氢氧根离子浓度增大,所以溶液的pH增大,故D错误;
故选C.
B.用石墨作电极电解H2SO4溶液时,阳极上氢氧根离子放电、阴极上氢离子放电,所以实质上是电解水,硫酸的物质的量不变,溶液体积减小,则溶液中硫酸浓度增大,溶液的pH减小,故B错误;
C.用石墨电极电解硫酸钠溶液时,阳极上氢氧根离子放电、阴极上氢离子放电,所以实质上是电解水,硫酸钠的物质的量不变,溶液体积减小,硫酸钠的浓度增大,但硫酸钠溶液呈中性,所以溶液的PH不变,故C正确;
D.用石墨作电极电解NaCl溶液时,阳极上氯离子放电、阴极上氢离子放电,导致溶液中有氢氧根离子生成,则溶液中氢氧根离子浓度增大,所以溶液的pH增大,故D错误;
故选C.
点评:本题考查了电解原理,明确离子放电顺序是解本题关键,根据电池反应式确定溶液中氢离子或氢氧根离子浓度变化,从而确定溶液酸碱性变化,题目难度不大.

练习册系列答案
相关题目
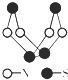 现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.其中如图是已经合成的最著名的硫-氮化合物的分子结构.下列说法正确的是( )
现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.其中如图是已经合成的最著名的硫-氮化合物的分子结构.下列说法正确的是( )| A、该物质的分子式为SN |
| B、该物质的晶体中微粒间作用力有2种 |
| C、该物质具有很高的熔、沸点 |
| D、该物质与化合物S2N2互为同素异形体 |
下列说法中正确的是( )
| A、凡能发生银镜反应的有机物一定是醛 |
| B、在氧气中燃烧时只生成CO2和H2O的物质一定是烃 |
| C、苯酚有弱酸性,俗称石炭酸,因此它是一种羧酸 |
| D、在酯化反应中,羧酸脱去羧基中的羟基,醇脱去羟基中的氢而生成水和酯 |
将a moL/L的Na2CO3溶液与b mol/L的NaHCO3溶液等体积混合,所得溶液中粒子浓度间的关系及相关判断不正确的是( )
| A、c(Na+)+c(H+)>c(CO32-)+c(HCO3-)+c(OH-) |
| B、c(Na+)>c(CO32-)+c(HCO3-)+c(H2CO3) |
| C、若a=b则可确定c(CO32-)+2c(OH-)=2c(H+)+c(HCO3-)+3c(H2CO3) |
| D、若c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+),则一定a<b |
4-甲基-2-乙基-1-戊烯,经加氢后其产物正确的名称是( )
| A、4-甲基-2-乙基戊烷 |
| B、2,5-二甲基己烷 |
| C、2,4-二甲基己烷 |
| D、2-乙基-4-甲基戊烷 |