题目内容
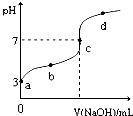 已知常温下CH3COOH的电离平衡常数为Ka,常温下,向20mL 0.1mol?L-1 CH3COOH溶液中逐滴加入0.1mol?L-1NaOH溶液,其pH变化曲线如图所示(忽略温度变化).下列说法中正确的是( )
已知常温下CH3COOH的电离平衡常数为Ka,常温下,向20mL 0.1mol?L-1 CH3COOH溶液中逐滴加入0.1mol?L-1NaOH溶液,其pH变化曲线如图所示(忽略温度变化).下列说法中正确的是( )| A、a点表示的溶液中由水电离出的H+浓度为1.0×10-3mol?L-1 | ||
| B、b点表示的溶液c(CH3COO-)<c(Na+) | ||
| C、c点表示CH3COOH和NaOH恰好反应完全 | ||
D、b、d点表示的溶液中
|
分析:A.先根据pH求出酸电离出的氢离子的浓度为c(H+)=10-pHmol/L,C酸能抑制水的电离,根据溶液中水的离子积表达式来计算;
B.根据溶液中的电荷守恒来分析;
C、根据醋酸和氢氧化钠生成盐的类型判断恰好反应时溶液的酸碱性来解答;
D、电离平衡常数只与温度有关,与其它任何条件都无关.
B.根据溶液中的电荷守恒来分析;
C、根据醋酸和氢氧化钠生成盐的类型判断恰好反应时溶液的酸碱性来解答;
D、电离平衡常数只与温度有关,与其它任何条件都无关.
解答:解:A.a点是c(H+)=10-pHmol/L=10-3mol/L,根据Kw=c(H+)?c(OH-),得溶液中的c(OH-)水=
=10-11mol/L=c(H+)水,故A错误;
B.溶液中电荷守恒:c(Na+)+c(H+)=c(OH-)+c(CH3COO-),b点时,c(H+)>c(OH-),则有c(CH3COO-)>c(Na+),故B错误;
C、醋酸和氢氧化钠反应生成醋酸钠,醋酸钠是强碱弱酸盐其水溶液呈碱性,当酸碱恰好反应时溶液应该呈碱性,但C点溶液呈中性,说明酸过量,故C错误;
D、b、d两点溶液的温度相同,所以b、d点表示的溶液中
均等于Ka,故D正确;
故选:D.
| 1×10-14 |
| 10-3 |
B.溶液中电荷守恒:c(Na+)+c(H+)=c(OH-)+c(CH3COO-),b点时,c(H+)>c(OH-),则有c(CH3COO-)>c(Na+),故B错误;
C、醋酸和氢氧化钠反应生成醋酸钠,醋酸钠是强碱弱酸盐其水溶液呈碱性,当酸碱恰好反应时溶液应该呈碱性,但C点溶液呈中性,说明酸过量,故C错误;
D、b、d两点溶液的温度相同,所以b、d点表示的溶液中
| c(CH3COO-)?c(H+) |
| c(CH3COOH) |
故选:D.
点评:本题考查了水的离子积的计算、酸碱混合的定性判断,电荷守恒的运用,题目难度中等,注意平衡常数K只与温度有关.

练习册系列答案
相关题目
已知常温下CH3COOH的电离平衡常数为Ka,常温下,向20mL 0.1 mol·L-1CH3COOH溶液中逐滴加入0.1 mol·L-1NaOH溶液,其pH变化曲线如图所示(忽视温度变化)。下列说法中错误的是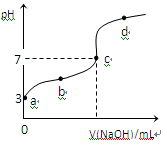
| A.a点表示的溶液中由水电离出的H+浓度为1.0×10-11 mol·L-1 |
| B.b点表示的溶液c(CH3COO-) > c(Na+) |
| C.c点表示CH3COOH和NaOH恰好反应完全 |
D.b、d点表示的溶液中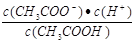 相等 相等 |
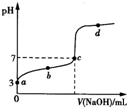 已知常温下CH3COOH的电离平衡常数为K.该温度下向20mL 0.1 mol?L-1 CH3COOH溶液中逐滴加入0.1 mol?L-1 NaOH溶液,其pH变化曲线如图所示(忽略温度变化).下列说法中不正确的是( )
已知常温下CH3COOH的电离平衡常数为K.该温度下向20mL 0.1 mol?L-1 CH3COOH溶液中逐滴加入0.1 mol?L-1 NaOH溶液,其pH变化曲线如图所示(忽略温度变化).下列说法中不正确的是( )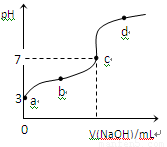
 相等
相等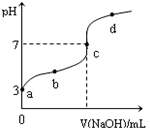
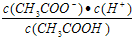 相等
相等