��Ŀ����
3����֪A��B��C��E����ɫ��Ӧ��Ϊ��ɫ������B������ʳƷ������A��B�����ʵ���֮��Ϊ1��1��ϲ���������ˮ�У��õ�����Һ��ֻ����һ�����ʣ�XΪһ�ֺ�ɫ���嵥�ʣ��ж���ͬ�������壬��������������ѭ����Ϊ�������壮GΪұ������ԭ�ϣ�G���������еõ����ֻ����A��H֮�������µ�ת����ϵ����������δд������
��1��д���������ʵĻ�ѧʽ��ANaOH��FFe��
��2��B��C��Ӧ�õ���״���µ�11.2L D�������D�ķ�Ӧ�У�ת�Ƶ��ӵ����ʵ���Ϊ1 mol��
��3��д��A+B��E�����ӷ���ʽ��HCO3-+OH-�TCO32-+H2O��
���� A��B��C��E����ɫ��Ӧ��Ϊ��ɫ�������������ж�����NaԪ�أ�����B������ʳƷ������A��B�����ʵ���֮��Ϊ1��1��ϲ���������ˮ�У��õ�����Һ��ֻ����һ�����ʣ���BΪNaHCO3��AΪNaOH��EΪNa2CO3��XΪһ�ֺ�ɫ���嵥�ʣ��ж���ͬ�������壬��������������ѭ����Ϊ�������壬������Ϊ������̼����XΪC��X������D�ķ�Ӧ������E��Na2CO3����Ӧ����B��NaHCO3������DΪO2��GΪұ������ԭ�ϣ�G���������еõ����ֻ������GΪFe3O4��D��F��ȼ����G����FΪ����Fe��B��C��Ӧ����D��O2������CΪNa2O2���ݴ˽��н��
��� �⣺A��B��C��E����ɫ��Ӧ��Ϊ��ɫ�������������ж�����NaԪ�أ�����B������ʳƷ������A��B�����ʵ���֮��Ϊ1��1��ϲ���������ˮ�У��õ�����Һ��ֻ����һ�����ʣ���BΪNaHCO3��AΪNaOH��EΪNa2CO3��XΪһ�ֺ�ɫ���嵥�ʣ��ж���ͬ�������壬��������������ѭ����Ϊ�������壬������Ϊ������̼����XΪC��X������D�ķ�Ӧ������E��Na2CO3����Ӧ����B��NaHCO3������DΪO2��GΪұ������ԭ�ϣ�G���������еõ����ֻ������GΪFe3O4��D��F��ȼ����G����FΪ����Fe��B��C��Ӧ����D��O2������CΪNa2O2��
��1�����ݷ�����֪��AΪNaOH��FΪFe��
�ʴ�Ϊ��NaOH��Fe��
��2��BΪNaHCO3��CΪNa2O2��DΪO2����Ӧ�õ���״���µ�11.2L���������������ʵ���Ϊ��$\frac{11.2L}{22.4L/mol}$=0.5mol��������������Ԫ�صĻ��ϼ�Ϊ-1�ۣ�������0��5mol����ת����1mol���ӣ�
�ʴ�Ϊ��1��
��3��A+B��EΪ̼���������������Ʒ�Ӧ����̼���ƺ�ˮ���÷�Ӧ�����ӷ���ʽΪ��HCO3-+OH-�TCO32-+H2O��
�ʴ�Ϊ��HCO3-+OH-�TCO32-+H2O��
���� ���⿼�����ƶϣ���Ŀ�Ѷ��еȣ����������Ϣ�ƶ���������Ϊ���ؼ���ע���������ճ���Ԫ�ؼ��仯�������ʣ��������������ѧ���ķ���������������������

��֪�������������ӵ�ͬһ��̼�ϲ��ȶ����ᷢ����Ӧ��-C��OH��2-��-CO-+H2O��
����������
| ����B�Ľṹ��ʽ | A����Է������� | ���ϸ�������A��CxHyOz����ͬ���칹����Ŀ | д��A������һ�ֽṹ��ʽ | |
| �� | ||||
| �� |
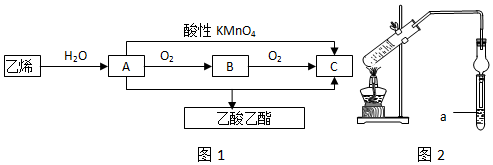
 �л���A�IJ����Ǻ���һ������ʯ��ҵ��չˮƽ�ı�־���ɷ�������ϵ��ת����B��D�������г����������л������˵��������ǣ�������
�л���A�IJ����Ǻ���һ������ʯ��ҵ��չˮƽ�ı�־���ɷ�������ϵ��ת����B��D�������г����������л������˵��������ǣ�������| A�� | A�Ľṹ��ʽΪCH2=CH2 | |
| B�� | 1molB���ʿ���������Na��Ӧ����0.5molH2 | |
| C�� | B��D��E�����ʿ����ñ���Na2CO3ŨҺ���� | |
| D�� | ��B��D�Ʊ�Eʱ��ŨH2SO4����������ˮ�� |
| A�� | ��ʯīΪ�缫���MgCl2��Һ��2Cl-+2H2O$\frac{\underline{\;ͨ��\;}}{\;}$ Cl2+H2��+2OH- | |
| B�� | ��ĭ���������ʱ��ѧ��Ӧ��2Al3++3CO32-+6H2O=Al��OH��3��+3CO2�� | |
| C�� | KI��Һ�е���ϡ���ᣬ��������4H++4I-+O2�T2I2+2H2O | |
| D�� | ��NH4HCO3��Һ�мӹ�����NaOH��Һ�����ȣ�NH4++OH-$\frac{\underline{\;\;��\;\;}}{\;}$NH3��+H2O |
| A�� |  �ⶨ�кͷ�Ӧ�ķ�Ӧ�� | B�� |  ʵ������ȡ������ | ||
| C�� |  ʵ������ȡ�������� | D�� |  ��ȥ�����л��е���ϩ |
 ��
�� �� ${\;}_{17}^{35}$Cl��${\;}_{17}^{37}$Cl֮��Ĺ�ϵ��ͬλ�أ�
�� ${\;}_{17}^{35}$Cl��${\;}_{17}^{37}$Cl֮��Ĺ�ϵ��ͬλ�أ�