题目内容
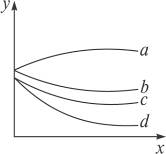
有等体积、等物质的量浓度的氢硫酸、亚硫酸溶液各两份,分别通入Cl2、O2,溶液的pH(y)与通入气体的物质的量(x)的关系如右图所示。则a、b、c、d能代表pH变化的反应正确?的是( )
A.a为氢硫酸中通入O2 B.b为亚硫酸中通入O2
C.c为氢硫酸中通入Cl2 D.d为亚硫酸中通入Cl2
AD
解析:
由于H2SO3是中强酸,H2S是弱酸,因此a、b的起点表示H2S的pH,c、d的起点表示H2SO3的pH。a、b中2H2S+O2====2H2O+2S↓,H2S+Cl2====2HCl+S↓,前者最后溶液呈中性使pH增大,后者生成强酸使pH减小;c、d中2H2SO3+O2====2H2SO4,H2SO3+Cl2+H2O==== H2SO4+2HCl,前者1 mol H2SO3,经反应生成2 mol H+,溶液pH减小,后者1 mol H2SO3经反应生成4 mol H+(H2SO4、HCl各提供2 mol),溶液pH减小得更多。

(13分)现有A、B、C、D、E五种强电解质,它们在水中可电离产生下列离子(各种离子不重复)。
| 阳离子 | H+、Na+、A13+、Ag+、Ba2+ |
| 阴离子 | OH—、C1—、CO32—、NO3—、SO42— |
已知:
①A、B两溶液呈碱性;C、D、E溶液呈酸性。
②A溶液与E溶液反应既有气体又有沉淀产生;A溶液与C溶液反应只有气体产生(沉淀包括微溶物,下同)。
③D溶液与另外四种溶液反应都能产生沉淀;C只能与D反应产生沉淀。
试回答下列问题:
(1)分别写出A、B、C、D、E的化学式:A 、B 、C 、
D 、E ;
(2)写出A、E反应的离子方程式: ;
(3)将C溶液逐滴加入等体积、等物质的量浓度的A溶液中,反应后溶液中各种离子浓度由大到小的顺序为: 。
(4)已知:NaOH(aq)+HNO3(aq)=NaNO3(aq)+H2O(1);△H =-Q kJ·mol-1。
写出B与C稀溶液反应的热化学方程式 。
(5)在100 mL 0.1 mol·L-1 E溶液中,逐滴加入40 mL 1.6 mol·L-1 NaOH溶液,最终得到沉淀物质的量为 mol。
(13分)现有A、B、C、D、E五种强电解质,它们在水中可电离产生下列离子(各种离子不重复)。
| 阳离子 | H+、Na+、A13+、Ag+、Ba2+ |
| 阴离子 | OH—、C1—、CO32—、NO3—、SO42— |
①A、B两溶液呈碱性;C、D、E溶液呈酸性。
②A溶液与E溶液反应既有气体又有沉淀产生;A溶液与C溶液反应只有气体产生(沉淀包括微溶物,下同)。
③D溶液与另外四种溶液反应都
 能产生沉淀;C只能与D反应产生沉淀。
能产生沉淀;C只能与D反应产生沉淀。试回答下列问题:
(1)分别写出A、B、C、D、E的化学式:A 、B 、C 、
D 、E ;
(2)写出A、E反应的离子方程式: ;
(3)将C溶液逐滴加入等体积、等物质的量浓度的A溶液中,反应后溶液中各种离子浓度由大到小的顺序为:
 。
。(4)已知:NaOH(aq)+HNO3(aq)=NaNO3(aq)+H2O(1);△H =-Q kJ·mol-1。
写出B与C稀溶液反应
 的热化学方程式 。
的热化学方程式 。(5)在100 mL 0.1 mol·L-1 E溶液中,逐滴加入40 mL 1.6 mol·L-1 NaOH溶液,最终得到沉淀物质的量为 mol。
(13分)现有A、B、C、D、E五种强电解质,它们在水中可电离产生下列离子(各种离子不重复)。
|
阳离子 |
H+、Na+、A13+、Ag+、Ba2+ |
|
阴离子 |
OH—、C1—、CO32—、NO3—、SO42— |
已知:
①A、B两溶液呈碱性;C、D、E溶液呈酸性。
②A溶液与E溶液反应既有气体又有沉淀产生;A溶液与C溶液反应只有气体产生(沉淀包括微溶物,下同)。
③D溶液与另外四种溶液反应都能产生沉淀;C只能与D反应产生沉淀。
试回答下列问题:
(1)分别写出A、B、C、D、E的化学式:A 、B 、C 、
D 、E ;
(2)写出A、E反应的离子方程式: ;
(3)将C溶液逐滴加入等体积、等物质的量浓度的A溶液中,反应后溶液中各种离子浓度由大到小的顺序为: 。
(4)已知:NaOH(aq)+HNO3(aq)=NaNO3(aq)+H2O(1);△H =-Q kJ·mol-1。
写出B与C稀溶液反应的热化学方程式 。
(5)在100 mL 0.1 mol·L-1 E溶液中,逐滴加入40 mL 1.6 mol·L-1 NaOH溶液,最终得到沉淀物质的量为 mol。