��Ŀ����
��ͼ���мס�����������������ɱ䣬ѹǿ���䣬�ұ���������䣮���������зֱ����1mol A��3mol B����ʱ�����������Ϊ0.5L���¶�ΪT�棬�����¶Ȳ��䷢����Ӧ��A��g��+3B��g��?xC��g��+2D��s�����������з�Ӧ��4min����n��A��=0.5mol��v��c��=0.5mol?L-1?min-1����1����ѧ����ʽ��xֵΪ______��������Ӧ��Ũ��ʱ��ƽ�����ƣ�kֵ______�����������С�����䡱����
��2������ѡ���У��ܱ������������������з�Ӧһ���ﵽƽ��״̬����______
A���������������ʵ�������ʱ��ı� B��v����A��=3v����B��
C��A��B��ת������� D������D����������ʱ��ı�
��3��t min��������з�Ӧ��ƽ�⣬���C��Ũ��Ϊ2mol?L-1����ʱ���������Ϊ______mL��B��ת���ʦ�����B��Ϊ______
��4����������B��ת����Ϊ������B��______������B�������������������=����

���𰸡���������1������v=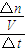 ����v��A������������֮�ȵ��ڻ�ѧ������֮�ȼ���x��
����v��A������������֮�ȵ��ڻ�ѧ������֮�ȼ���x��
��ѧƽ�ⳣ��ֻ���¶�Ӱ�죬��Ũ���أ�
��2�����ݻ�ѧƽ��״̬����������������Ӧ�ﵽƽ��״̬ʱ�����淴Ӧ������ȣ������ʵ�Ũ�ȡ���������������Լ��ٷֺ������䣬�Լ��ɴ�������һЩ��Ҳ�������仯��
��3���������з�Ӧ��4min����n��A��=0.5mol��v��c��=0.5mol?L-1?min-1����v��A��= =0.25mol?L-1?min-1����x=2��������ɱ䣬ѹǿ�����¶Ȳ��䣬��Ӧǰ�����������Ũ����ȣ���λ����ں��еĻ����������ʵ�����ȣ�����ʼ����1molA��3molB�����Ϊ0.5L����ʼ����������Ũ��Ϊ
=0.25mol?L-1?min-1����x=2��������ɱ䣬ѹǿ�����¶Ȳ��䣬��Ӧǰ�����������Ũ����ȣ���λ����ں��еĻ����������ʵ�����ȣ�����ʼ����1molA��3molB�����Ϊ0.5L����ʼ����������Ũ��Ϊ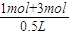 =8mol/L��ƽ���C��Ũ��Ϊ2mol/L����ƽ��ʱA��B���ܵ�Ũ��Ϊ8mol/L-2mol/L=6mol/L�����ڿ�ʼ����1molA��3molB����A��B��1��3��Ӧ������ƽ��ʱA��B��Ũ�ȱ�Ϊ1��3������ƽ��ʱc��A��=
=8mol/L��ƽ���C��Ũ��Ϊ2mol/L����ƽ��ʱA��B���ܵ�Ũ��Ϊ8mol/L-2mol/L=6mol/L�����ڿ�ʼ����1molA��3molB����A��B��1��3��Ӧ������ƽ��ʱA��B��Ũ�ȱ�Ϊ1��3������ƽ��ʱc��A��= ×6mol/L=1.5mol/L��c��B��=6mol/L-1.5mol/L=4.5mol/L������A��B��Ũ�ȣ�������CΪnmol����������ʽ��ʾ����������ʵ����仯��ƽ��ʱ����ֵ����ʵ���������A��C��Ũ�ȹ�ϵ�з��̼���n��ֵ������V=
×6mol/L=1.5mol/L��c��B��=6mol/L-1.5mol/L=4.5mol/L������A��B��Ũ�ȣ�������CΪnmol����������ʽ��ʾ����������ʵ����仯��ƽ��ʱ����ֵ����ʵ���������A��C��Ũ�ȹ�ϵ�з��̼���n��ֵ������V=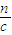 ���㷴Ӧ�����������ת���ʵ��ڼ���B��ת���ʣ�
���㷴Ӧ�����������ת���ʵ��ڼ���B��ת���ʣ�
��4���ɷ�Ӧ��֪����Ӧǰ�����������С��������ѹǿ��С����ѹǿ���䣬ѹǿ����ƽ���������С�ķ����ƶ�����������Ӧ�ƶ����ݴ��ж�ת���ʣ�
����⣺��1���������з�Ӧ��4min����n��A��=0.5mol��v��c��=0.5mol?L-1?min-1����v��A��=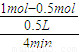 =0.25mol?L-1?min-1��1��x=0.25mol?L-1?min-1��0.5mol?L-1?min-1�ʣ���x=2��
=0.25mol?L-1?min-1��1��x=0.25mol?L-1?min-1��0.5mol?L-1?min-1�ʣ���x=2��
��ѧƽ�ⳣ��ֻ���¶�Ӱ�죬��Ũ���أ�������Ӧ��Ũ��ʱ��kֵ���䣬
�ʴ�Ϊ��2�����䣻
��2��A����Ӧ�й������ɣ������淴Ӧ���������������С��������������������ʱ��ı䣬˵������ƽ�⣬��A��ȷ��
B����ͬ���ʱ�ʾ���淴Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ�˵����Ӧ����ƽ�⣮v����A��=3v����B������v����A����v����B��=1��3�����ڻ�ѧ������֮��1��3��˵������ƽ�⣬��B��ȷ��
C����ʼ���������зֱ����1molA��3molB����A��B��1��3��Ӧ�������Ƿ�ƽ��A��B��ת������ʼ���ն���ȣ���C����
D���淴Ӧ���������������С������D������������D����������ʱ��ı䣬˵������ƽ�⣬��D��ȷ��
��ѡ��ABD��
��3��������ɱ䣬ѹǿ�¶Ȳ��䣬��Ӧǰ�����������Ũ����ȣ���λ����ں��еĻ����������ʵ�����ȣ�����ʼ����1molA��3molB�����Ϊ0.5L����ʼ����������Ũ��Ϊ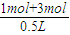 =8mol/L��
=8mol/L��
ƽ���C��Ũ��Ϊ2mol/L����ƽ��ʱA��B���ܵ�Ũ��Ϊ8mol/L-2mol/L=6mol/L�����ڿ�ʼ����1molA��3molB����A��B��1��3��Ӧ������ƽ��ʱA��B��Ũ�ȱ�Ϊ1��3������ƽ��ʱc��A��= ×6mol/L=1.5mol/L��c��B��=6mol/L-1.5mol/L=4.5mol/L��
×6mol/L=1.5mol/L��c��B��=6mol/L-1.5mol/L=4.5mol/L��
������CΪnmol����
A��g��+3B��g��?2C��g��+D��s��
��ʼ��mol����1 3 0
�仯��mol����n 3n 2n
ƽ�⣨mol����1-n 3-3n 2n
���ԣ�1-n����2n=1.5mol/L��2mol/L�����n=0.4��
��ƽ�������Ϊ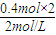 =0.4L=400mL��
=0.4L=400mL��
����B��ת���ʦ�����B��=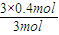 ×100%=40%��
×100%=40%��
�ʴ�Ϊ��400��40%��
��3����ѹǿ��С����ѹǿ���䣬�ױ���ѹǿ��Ӧǰ�����������С���ױ���ѹǿ��ѹǿ����ƽ���������С�ķ����ƶ�����������Ӧ�ƶ������Լ���B��ת���ʱ����еĴ�������B����������B�����ʴ�Ϊ������
���������⿼�黯ѧƽ����йؼ��㡢Ӱ��ƽ�������ء�ƽ��״̬�жϵȣ��Ѷ��еȣ���3��Ϊ�״��㣬ȷ����Ӧǰ���������ܵ����ʵ���Ũ�Ȳ����ǹؼ���
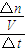 ����v��A������������֮�ȵ��ڻ�ѧ������֮�ȼ���x��
����v��A������������֮�ȵ��ڻ�ѧ������֮�ȼ���x����ѧƽ�ⳣ��ֻ���¶�Ӱ�죬��Ũ���أ�
��2�����ݻ�ѧƽ��״̬����������������Ӧ�ﵽƽ��״̬ʱ�����淴Ӧ������ȣ������ʵ�Ũ�ȡ���������������Լ��ٷֺ������䣬�Լ��ɴ�������һЩ��Ҳ�������仯��
��3���������з�Ӧ��4min����n��A��=0.5mol��v��c��=0.5mol?L-1?min-1����v��A��=
 =0.25mol?L-1?min-1����x=2��������ɱ䣬ѹǿ�����¶Ȳ��䣬��Ӧǰ�����������Ũ����ȣ���λ����ں��еĻ����������ʵ�����ȣ�����ʼ����1molA��3molB�����Ϊ0.5L����ʼ����������Ũ��Ϊ
=0.25mol?L-1?min-1����x=2��������ɱ䣬ѹǿ�����¶Ȳ��䣬��Ӧǰ�����������Ũ����ȣ���λ����ں��еĻ����������ʵ�����ȣ�����ʼ����1molA��3molB�����Ϊ0.5L����ʼ����������Ũ��Ϊ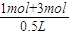 =8mol/L��ƽ���C��Ũ��Ϊ2mol/L����ƽ��ʱA��B���ܵ�Ũ��Ϊ8mol/L-2mol/L=6mol/L�����ڿ�ʼ����1molA��3molB����A��B��1��3��Ӧ������ƽ��ʱA��B��Ũ�ȱ�Ϊ1��3������ƽ��ʱc��A��=
=8mol/L��ƽ���C��Ũ��Ϊ2mol/L����ƽ��ʱA��B���ܵ�Ũ��Ϊ8mol/L-2mol/L=6mol/L�����ڿ�ʼ����1molA��3molB����A��B��1��3��Ӧ������ƽ��ʱA��B��Ũ�ȱ�Ϊ1��3������ƽ��ʱc��A��= ×6mol/L=1.5mol/L��c��B��=6mol/L-1.5mol/L=4.5mol/L������A��B��Ũ�ȣ�������CΪnmol����������ʽ��ʾ����������ʵ����仯��ƽ��ʱ����ֵ����ʵ���������A��C��Ũ�ȹ�ϵ�з��̼���n��ֵ������V=
×6mol/L=1.5mol/L��c��B��=6mol/L-1.5mol/L=4.5mol/L������A��B��Ũ�ȣ�������CΪnmol����������ʽ��ʾ����������ʵ����仯��ƽ��ʱ����ֵ����ʵ���������A��C��Ũ�ȹ�ϵ�з��̼���n��ֵ������V=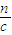 ���㷴Ӧ�����������ת���ʵ��ڼ���B��ת���ʣ�
���㷴Ӧ�����������ת���ʵ��ڼ���B��ת���ʣ���4���ɷ�Ӧ��֪����Ӧǰ�����������С��������ѹǿ��С����ѹǿ���䣬ѹǿ����ƽ���������С�ķ����ƶ�����������Ӧ�ƶ����ݴ��ж�ת���ʣ�
����⣺��1���������з�Ӧ��4min����n��A��=0.5mol��v��c��=0.5mol?L-1?min-1����v��A��=
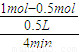 =0.25mol?L-1?min-1��1��x=0.25mol?L-1?min-1��0.5mol?L-1?min-1�ʣ���x=2��
=0.25mol?L-1?min-1��1��x=0.25mol?L-1?min-1��0.5mol?L-1?min-1�ʣ���x=2����ѧƽ�ⳣ��ֻ���¶�Ӱ�죬��Ũ���أ�������Ӧ��Ũ��ʱ��kֵ���䣬
�ʴ�Ϊ��2�����䣻
��2��A����Ӧ�й������ɣ������淴Ӧ���������������С��������������������ʱ��ı䣬˵������ƽ�⣬��A��ȷ��
B����ͬ���ʱ�ʾ���淴Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ�˵����Ӧ����ƽ�⣮v����A��=3v����B������v����A����v����B��=1��3�����ڻ�ѧ������֮��1��3��˵������ƽ�⣬��B��ȷ��
C����ʼ���������зֱ����1molA��3molB����A��B��1��3��Ӧ�������Ƿ�ƽ��A��B��ת������ʼ���ն���ȣ���C����
D���淴Ӧ���������������С������D������������D����������ʱ��ı䣬˵������ƽ�⣬��D��ȷ��
��ѡ��ABD��
��3��������ɱ䣬ѹǿ�¶Ȳ��䣬��Ӧǰ�����������Ũ����ȣ���λ����ں��еĻ����������ʵ�����ȣ�����ʼ����1molA��3molB�����Ϊ0.5L����ʼ����������Ũ��Ϊ
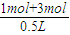 =8mol/L��
=8mol/L��ƽ���C��Ũ��Ϊ2mol/L����ƽ��ʱA��B���ܵ�Ũ��Ϊ8mol/L-2mol/L=6mol/L�����ڿ�ʼ����1molA��3molB����A��B��1��3��Ӧ������ƽ��ʱA��B��Ũ�ȱ�Ϊ1��3������ƽ��ʱc��A��=
 ×6mol/L=1.5mol/L��c��B��=6mol/L-1.5mol/L=4.5mol/L��
×6mol/L=1.5mol/L��c��B��=6mol/L-1.5mol/L=4.5mol/L��������CΪnmol����
A��g��+3B��g��?2C��g��+D��s��
��ʼ��mol����1 3 0
�仯��mol����n 3n 2n
ƽ�⣨mol����1-n 3-3n 2n
���ԣ�1-n����2n=1.5mol/L��2mol/L�����n=0.4��
��ƽ�������Ϊ
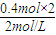 =0.4L=400mL��
=0.4L=400mL������B��ת���ʦ�����B��=
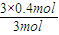 ×100%=40%��
×100%=40%���ʴ�Ϊ��400��40%��
��3����ѹǿ��С����ѹǿ���䣬�ױ���ѹǿ��Ӧǰ�����������С���ױ���ѹǿ��ѹǿ����ƽ���������С�ķ����ƶ�����������Ӧ�ƶ������Լ���B��ת���ʱ����еĴ�������B����������B�����ʴ�Ϊ������
���������⿼�黯ѧƽ����йؼ��㡢Ӱ��ƽ�������ء�ƽ��״̬�жϵȣ��Ѷ��еȣ���3��Ϊ�״��㣬ȷ����Ӧǰ���������ܵ����ʵ���Ũ�Ȳ����ǹؼ���

��ϰ��ϵ�д�
�����Ŀ
 ��ͼ���мס�����������������ɱ䣬ѹǿ���䣬�ұ���������䣮���������зֱ����1mol A��3mol B����ʱ�����������Ϊ0.5L���¶�ΪT�棬�����¶Ȳ��䷢����Ӧ��A��g��+3B��g��?xC��g��+2D��s�����������з�Ӧ��4min����n��A��=0.5mol��v��c��=0.5mol?L-1?min-1��
��ͼ���мס�����������������ɱ䣬ѹǿ���䣬�ұ���������䣮���������зֱ����1mol A��3mol B����ʱ�����������Ϊ0.5L���¶�ΪT�棬�����¶Ȳ��䷢����Ӧ��A��g��+3B��g��?xC��g��+2D��s�����������з�Ӧ��4min����n��A��=0.5mol��v��c��=0.5mol?L-1?min-1��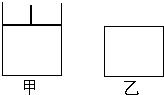 ��ͼ���мס�����������������ɱ�ѹǿ���䣬�ұ���������䣮���������зֱ����1molA��3molB����ʱ�����������Ϊ500mL���¶�ΪT�森�����¶Ȳ��䷢����Ӧ��
��ͼ���мס�����������������ɱ�ѹǿ���䣬�ұ���������䣮���������зֱ����1molA��3molB����ʱ�����������Ϊ500mL���¶�ΪT�森�����¶Ȳ��䷢����Ӧ��

