题目内容
某溶液中可能含有NH4+、Ba2+、Mg2+、Ag+、OH-、SO42-、CO32-中的某几种,现用该溶液做以下实验:①取此溶液少许,加入足量盐酸无明显现象;②另取少许加入足量浓氢氧化钠溶液,有白色沉淀生成;③将②中沉淀过滤,取滤液微热,有无色刺激性气味气体放出,该气体能使湿润的红色石蕊试纸变蓝。
由此推断,该溶液中肯定有 离子,肯定没有 离子。
写出②中发生反应的离子方程式 。
肯定存在NH4+、Mg2+SO42-肯定不存在的是Ba2+、Ag+OH-、CO32-
Mg2++2OH-=Mg(OH)2↓、NH4++OH-=NH3?H2O
解析试题分析:①取此溶液少许,加入足量盐酸无明显现象,说明溶液中不存在银离子、碳酸根离子;②另取少许加入足量浓氢氧化钠溶液,有白色沉淀生成,说明溶液中一定存在镁离子,一定不会存在碳酸根离子、氢氧根离子;③将②中沉淀过滤,取滤液微热,有无色刺激性气味气体放出,该气体能使湿润的红色石蕊试纸变蓝,该气体为氨气,溶液中一定存在铵离子,一定不会存在氢氧根离子,再根据溶液呈电中性判断,溶液中一定存在硫酸根离子,一定不会存在钡离子.(1)根据以上分析可知,该溶液中一定存在的离子有:NH4+、Mg2+ SO42-;一定不存在的离子为:Ba2+、Ag+ OH-、CO32-,故答案为:NH4+、Mg2+ SO42-;Ba2+、Ag+ OH-、CO32-;(2)以上信息中存在的反应有:镁离子与氢氧根离子生成氢氧化镁沉淀,离子方程式为:Mg2++2 OH-=Mg(OH)2↓,铵离子与氢氧根离子反应生成一水合氨,反应的离子方程式为:NH4++OH-=NH3?H2O,故答案为:Mg2++2 OH-=Mg(OH)2↓、NH4++OH-=NH3?H2O.
考点:离子反应、常见的离子检验方法

 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案下列各组离子或分子在溶液中能大量共存,且满足相应要求的是 (. )
| 选项 | 离子或分子 | 要求 |
| A | K+ 、NO3-、Cl-、HS- | c(K+)<c(Cl-) |
| B | Fe3+、NO3-、SO32-、Cl- | 滴加盐酸立即有气体产生 |
| C | NH4+、Al3+、SO42-、CH3COOH | 滴加NaOH溶液立即有气体产生 |
| D | Na+、HCO3-、Mg2+、SO42- | 逐滴滴加氨水立即有沉淀产生 |
某无色透明的酸性溶液中能大量共存的一组离子是( )
| A.Mg2+、Na+、SO42-、NO 3- | B.Na+、HCO3-、K+、SO42- |
| C.MnO4-、K+、SO42-、Na+ | D.NH4+、CO32-、Al3+、Cl- |
下列离子方程式对应的化学方程式正确的是
| A.H++OH-=H2O CH3COOH+NaOH=CH3COONa+H2O |
| B.Ba2++SO42-=BaSO4↓Ba(OH)2+H2SO4=BaSO4↓+2H2O |
| C.CO32-+2H+=CO2↑+H2O CaCO3+2HCl=CaCl2+CO2↑+H2O |
| D.3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O |
下列反应的离子方程式正确的是
| A.向Fe(NO3)2稀溶液中加入盐酸:3Fe2++4H++NO3-=3Fe3++NO↑+2H2O |
| B.铜片加入浓硝酸中:3Cu+4H++NO3-=3Cu2++NO↑+2H2O |
C.碳酸氢铵溶液与足量的NaOH溶液混合后加热:NH4++OH- NH3↑+H2O NH3↑+H2O |
| D.AlCl3溶液中加入足量氨水:Al3++4NH3·H2O=AlO2-+4NH4++2H2O |
能正确表示下列反应的离子方程式是
| A.NaHCO3的水解:HCO3-+H2O=CO32-+H3O+ |
| B.用银氨溶液检验乙醛的醛基: CH3CHO+2Ag(NH3)2OH  CH3COO-+NH4++3NH3+2Ag↓+H2O CH3COO-+NH4++3NH3+2Ag↓+H2O |
C.向苯酚钠溶液中通入少量的CO2:CO2+H2O+2C6H5O- 2C6H5OH+2CO32- 2C6H5OH+2CO32- |
| D.泡沫灭火剂的原理:Al3++3HCO3-=Al(OH)3↓+3CO2↑ |
下列化学反应的离子方程式正确的是
| A.FeCl3与氨水反应:Fe3++3NH3·H2O=Fe(OH)3↓+3NH4+ |
B.铜与稀硝酸反应:Cu+8H++2NO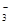 =Cu2++2NO↑+4H2O =Cu2++2NO↑+4H2O |
| C.NO2与水反应:3NO2+H2O=NO3-+NO+2H+ |
| D.醋酸与CaCO3反应:CaCO3+2H+=Ca2++H2O+CO2↑ |
下列离子方程式正确的是
| A.硫酸铜溶液与足量氢氧化钡溶液混合:Ba2++SO42-=BaSO4↓ |
| B.AgCl悬浊液中加入硫化钠饱和溶液:2AgCl + S2-=Ag2S +2Cl- |
C.硫化钠的水解反应:S2-+H3O+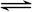 HS-+H2O HS-+H2O |
| D.用K37ClO3与浓盐酸制氯气:37ClO3-+6H++6Cl-=37Cl-+3Cl2↑+3H2O |
下列各组离子中,在强碱性溶液中能大量共存是
| A.Na+、HCO3-、CO32-、K+ | B.K+、Ba2+、Cl-、NO3- |
| C.Na+、NO3-、K+、S2- | D.K+、NH4+、SO42-、Cl- |