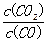题目内容
在一密闭容器中,CO和H2O混合加热到850℃达到下列平衡:
CO(g)+H2O(g) CO2(g)+H2(g),K=1.0,若反应开始时CO和H2O的浓度分别为0.20 mol/L和1.00 mol/L,则CO转化为CO2的转化率为
CO2(g)+H2(g),K=1.0,若反应开始时CO和H2O的浓度分别为0.20 mol/L和1.00 mol/L,则CO转化为CO2的转化率为
CO(g)+H2O(g)
 CO2(g)+H2(g),K=1.0,若反应开始时CO和H2O的浓度分别为0.20 mol/L和1.00 mol/L,则CO转化为CO2的转化率为
CO2(g)+H2(g),K=1.0,若反应开始时CO和H2O的浓度分别为0.20 mol/L和1.00 mol/L,则CO转化为CO2的转化率为| A.5% | B.80% | C.83% | D.91% |
C
CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
初始浓度:0.20 1.00 0 0
转化浓度: x x x x
平衡浓度:0.20-x 1.00-x x x
根据平衡常数计算公式可得:K=x2=(0.20-x)(1.00-x),求得x=1/6
故CO转化率为: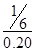 =83%
=83%
 CO2(g)+H2(g)
CO2(g)+H2(g)初始浓度:0.20 1.00 0 0
转化浓度: x x x x
平衡浓度:0.20-x 1.00-x x x
根据平衡常数计算公式可得:K=x2=(0.20-x)(1.00-x),求得x=1/6
故CO转化率为:
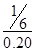 =83%
=83%
练习册系列答案
相关题目
 pC(g),在密闭容器中进行,下图表示在不同反应时间t、温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线,由曲线分析,下列判断正确的是
pC(g),在密闭容器中进行,下图表示在不同反应时间t、温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线,由曲线分析,下列判断正确的是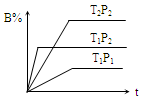
 CH3COO-+H+,请根据该平衡完成下列表格,电离平衡移动方向填“正方向”或“逆方向”,离子浓度的变化请用“增大”、“减小”或“不变”表示。
CH3COO-+H+,请根据该平衡完成下列表格,电离平衡移动方向填“正方向”或“逆方向”,离子浓度的变化请用“增大”、“减小”或“不变”表示。 N2O4,在此温度下,再向容器通入一定量NO2,重新建立平衡后,容器中NO2的体积分数 ( )
N2O4,在此温度下,再向容器通入一定量NO2,重新建立平衡后,容器中NO2的体积分数 ( ) CO(g)+H2O(g);△H=" Q" KJ/mol其化学平衡常数K和温度t的关系如下:
CO(g)+H2O(g);△H=" Q" KJ/mol其化学平衡常数K和温度t的关系如下: 2SO3(g)是制备硫酸的重要反应。下列叙述正确的是
2SO3(g)是制备硫酸的重要反应。下列叙述正确的是 C+D,增大压强时反应速率变化如下图所示。则下列关于各物质状态的说法正确的是
C+D,增大压强时反应速率变化如下图所示。则下列关于各物质状态的说法正确的是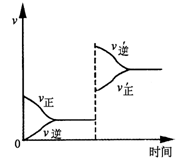
 p C(g) + q D(g)的反应中,(m.n.p. q为各物质的化学计量数),经5min达到平衡,测得:A增加3 mol·L-1,B增加1 mol·L-1,C减少2 mol·L-1,此时若给体系加压,平衡不移动,则m :n :p :q为
p C(g) + q D(g)的反应中,(m.n.p. q为各物质的化学计量数),经5min达到平衡,测得:A增加3 mol·L-1,B增加1 mol·L-1,C减少2 mol·L-1,此时若给体系加压,平衡不移动,则m :n :p :q为 Fe2O3(s)+CO(g)
Fe2O3(s)+CO(g)
 Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如下
Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如下