题目内容
【题目】某合作学习小组的同学利用下列氧化还原反应设计原电池:2KMnO4+10FeSO4+8H2SO4═2MnSO4+5Fe2(SO4)3+K2SO4+8H2O盐桥中装有饱和K2SO4溶液,下列叙述中正确的是( )
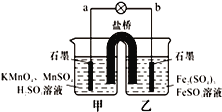
A. 外电路的电流方向是从a到b
B. 甲烧杯中溶液的pH逐渐减小
C. 电池工作时,盐桥中的SO42-移向甲烧杯
D. 乙烧杯中发生还原反应
【答案】A
【解析】
A.由上述分析可知,a为正极,b为负极,则电流从a到b,故A正确;B.甲烧杯中发生反应为:MnO4-+8H++5e-═Mn2++4H2O,氢离子浓度减小,导致溶液的pH增大,故B错误;C.阴离子向负极移动,则盐桥中的SO42-移向乙烧杯中,故C错误;D.甲烧杯中(a电极)发生还原反应,Mn元素的化合价降低,电极反应为MnO4-+8H++5e-═Mn2++4H2O,b电极亚铁离子失去电子发生氧化反应,故D错误;故答案为A。

【题目】下表为各物质中所含有的少量杂质,以及除去这些杂质应选用的试剂或操作方法.其中正确的是( )
选项 | A | B | C | D |
物质 | KNO3溶液 | CO2 | 水 | 乙醇 |
杂质 | KOH | H2O(g) | 溴 | 水 |
除杂试剂 | FeCl3溶液 | 浓硫酸 | 酒精 | 生石灰 |
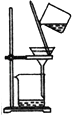
除杂装置 |
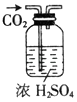
|
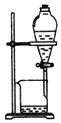
|
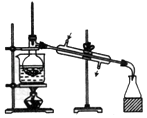
|
|
A.A
B.B
C.C
D.D
【题目】下列实验操作能达到实验目的的是
选项 | 实验目的 | 实验操作 |
A | 探究浓度对化学平衡的影响 | 向盛有2.5mL 0.005mol/L FeCl3,溶液的试管中加入2.5mL 0.015 mol/L KSCN溶液,再滴加4滴饱和FeCl3溶液 |
B | 从FeCl3溶液提取无水FeCl3 | 将FeCl3溶液灼烧蒸干 |
C | 证 明 Ksp(AgCl)>Ksp(AgI) | 在2mL 0.01 mol/LAgNO3溶液中滴加1mL0.01 mol/LHCl溶液,再滴加1mL 0.01 mol/LKI 溶液 |
D | 配制澄清的FeCl3浓溶液 | 将FeCl3固体置入少量水中搅拌 |
A. A B. B C. C D. D