题目内容
某1 mol链烃A在一定条件下完全裂化成1 mol烷烃B和1 mol烯烃C,生成的混合气体对H2的相对密度为14.5。试通过计算回答下列问题:
(1)写出链烃A可能的结构简式和名称。
(2)烷烃B和烯烃C可能各是什么物质?
(3)如果要求1 mol B完全燃烧时需要O2的物质的量是整数,那么C只能是什么烯烃?
(1)写出链烃A可能的结构简式和名称。
(2)烷烃B和烯烃C可能各是什么物质?
(3)如果要求1 mol B完全燃烧时需要O2的物质的量是整数,那么C只能是什么烯烃?
(1)CH3CH2CH2CH3,正丁烷或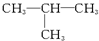 ,2-甲基丙烷
,2-甲基丙烷
(2)B:CH4 C:CH2==CHCH3或B:C2H6 C:CH2==CH2
(3)CH2==CHCH3
 ,2-甲基丙烷
,2-甲基丙烷(2)B:CH4 C:CH2==CHCH3或B:C2H6 C:CH2==CH2
(3)CH2==CHCH3
这是一道有关裂化知识的计算题。
关键在于裂化后生成物分别为烷烃和烯烃时,原物质必为烷烃。利用相对密度先求出A的相对分子质量,然后再推断其分子式。
设烷烃B的分子式为CmH2m+2,相对分子质量为Mr(B),烯烃C分子式为CnH2n,相对分子质量为M(C),根据质量守恒定律,可知链烃A的组成应为C(m+n)H(m+n)+2,符合烷烃的通式。依题意有:(1)Mr(A)= Mr(B)+ Mr(C),2×14.5×2=58,即 14(m+n)+2=58
得m+n=4
所以A的分子式为C4H10,其可能的结构如下:CH3CH2CH2CH3,正丁烷或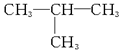 ,2-甲基丙烷。
,2-甲基丙烷。
(2)讨论m+n=4
当m=1时,n=3,即B为CH4,C为CH2==CHCH3;
当m=2时,n=2,即B为C2H6,C为CH2==CH2;
当m≥3时,n≤1,无意义。
(3)从B的燃烧反应方程式来看:CH4+2O2 CO2+2H2O
CO2+2H2O
C2H6+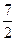 O2
O2 2CO2+3H2O
2CO2+3H2O
可知B应是CH4,则C只能是CH2==CHCH3。
关键在于裂化后生成物分别为烷烃和烯烃时,原物质必为烷烃。利用相对密度先求出A的相对分子质量,然后再推断其分子式。
设烷烃B的分子式为CmH2m+2,相对分子质量为Mr(B),烯烃C分子式为CnH2n,相对分子质量为M(C),根据质量守恒定律,可知链烃A的组成应为C(m+n)H(m+n)+2,符合烷烃的通式。依题意有:(1)Mr(A)= Mr(B)+ Mr(C),2×14.5×2=58,即 14(m+n)+2=58
得m+n=4
所以A的分子式为C4H10,其可能的结构如下:CH3CH2CH2CH3,正丁烷或
 ,2-甲基丙烷。
,2-甲基丙烷。(2)讨论m+n=4
当m=1时,n=3,即B为CH4,C为CH2==CHCH3;
当m=2时,n=2,即B为C2H6,C为CH2==CH2;
当m≥3时,n≤1,无意义。
(3)从B的燃烧反应方程式来看:CH4+2O2
 CO2+2H2O
CO2+2H2OC2H6+
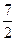 O2
O2 2CO2+3H2O
2CO2+3H2O可知B应是CH4,则C只能是CH2==CHCH3。

练习册系列答案
相关题目
 CO2+2H2O
CO2+2H2O