题目内容
纳米碳酸钙广泛应用于橡胶、塑料、造纸、化学建材、油墨、涂料、密封胶与胶粘剂等行业。在浓CaCl2溶液中通入NH3和CO2,可以制得纳米级碳酸钙。某校学生实验小组设计下图所示装置,制取该产品。D中装有蘸稀硫酸的脱脂棉,图中夹持装置已略去。
Ⅰ.可选用的药品有:
a.石灰石 b.饱和氯化钙溶液 c.6 mol/L盐酸 d.氯化铵 e.氢氧化钙

(1)A中制备气体时,所需药品是(选填字母序号) ;
(2)B中盛有饱和碳酸氢钠溶液,其作用是 ;
(3)写出制取氨气的化学方程式 ;
(4)在实验过程中,向C中通入气体是有先后顺序的,应先通入气体的化学式 ;
(5)检验D出口处是否有氨气逸出的方法是 ;
(6)写出制纳米级碳酸钙的化学方程式 。
(7)若实验过程中有氨气逸出,应选用下列 装置回收(填代号)。

Ⅱ.经分析在上述氯化铵样品中含有杂质碳酸氢钠。为了测定氯化铵的质量分数,该学生实验小组又设计了如下实验流程:

试回答:
(1)所加试剂A的化学式为
(2)B操作方法是
(3)样品中氯化铵的质量分数为 。
Ⅰ.(1)ac(1分)
(2)除去CO2中的HCl(1分)
(3)2NH4Cl + Ca(OH)2 CaCl2 + 2NH3↑+ 2H2O(2分)
CaCl2 + 2NH3↑+ 2H2O(2分)
(4)NH3(1分)
(5)将湿润的红色石蕊试纸放在D出口处,若试纸变蓝,则证明有氨气逸出;若试纸不变蓝,则证明没有氨气逸出。(或用蘸有浓盐酸的玻璃棒靠近D出口处,若有白烟,则证明有氨气逸出;若没有白烟,则证明没有氨气逸出。)(2分)
(6)CaCl2 + H2O + CO2 + 2NH3 = CaCO3 + 2NH4Cl(2分)
(7)b(1分)
Ⅱ.
(1)Ca(OH)2或Ba(OH)2 (1分)
(2)过滤(1分)
(3)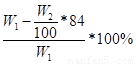 或
或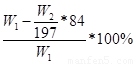
【解析】
试题分析:(1)根据题设条件中的装置图是固液不加热型装置,而且装置中带有分液漏斗,为制取二氧化碳的装置,根据二氧化碳的实验室制法,可知装置中盛放的是碳酸钙和稀盐酸,即选择a、b。(2)B中盛有饱和碳酸氢钠溶液,起到抑制二氧化碳溶解,除掉氯化氢的作用,原理是:CO2+H2O H2CO3
H2CO3 H++HCO3-,当溶液时饱和的碳酸氢钠溶液时,溶液中由于存在大量的碳酸氢根离子,是平衡左移,从而起到抑制二氧化碳溶解的作用。(3)制取氨气的化学方程式为:2NH4Cl + Ca(OH)2
H++HCO3-,当溶液时饱和的碳酸氢钠溶液时,溶液中由于存在大量的碳酸氢根离子,是平衡左移,从而起到抑制二氧化碳溶解的作用。(3)制取氨气的化学方程式为:2NH4Cl + Ca(OH)2  CaCl2 + 2NH3↑+ 2H2O。(4)在实验过程中,向C中通入气体应当先是NH3,原因是如果先通二氧化碳气体,由于氨气的密度小于二氧化碳,不能充分接触,造成氨气浪费的较多,因此,应先通入氨气,后通二氧化碳。(5)可根据氨气的化学性质进行证明,氨气能使湿润的红色石蕊试纸变蓝,也能和氯化氢发生反应,因此正确的答案为:将湿润的红色石蕊试纸放在D出口处,若试纸变蓝,则证明有氨气逸出;若试纸不变蓝,则证明没有氨气逸出。(或用蘸有浓盐酸的玻璃棒靠近D出口处,若有白烟,则证明有氨气逸出;若没有白烟,则证明没有氨气逸出。)
CaCl2 + 2NH3↑+ 2H2O。(4)在实验过程中,向C中通入气体应当先是NH3,原因是如果先通二氧化碳气体,由于氨气的密度小于二氧化碳,不能充分接触,造成氨气浪费的较多,因此,应先通入氨气,后通二氧化碳。(5)可根据氨气的化学性质进行证明,氨气能使湿润的红色石蕊试纸变蓝,也能和氯化氢发生反应,因此正确的答案为:将湿润的红色石蕊试纸放在D出口处,若试纸变蓝,则证明有氨气逸出;若试纸不变蓝,则证明没有氨气逸出。(或用蘸有浓盐酸的玻璃棒靠近D出口处,若有白烟,则证明有氨气逸出;若没有白烟,则证明没有氨气逸出。)
(6)根据题意和原子守恒可知,实际上该化学反应包括2个化学反应:⑴H2O + CO2 + 2NH3=(NH4)2CO3,⑵
(NH4)2CO3+CaCl2= CaCO3 + 2NH4Cl,最后将2个化学方程式合并,即得制纳米级碳酸钙的化学方程式为:CaCl2 + H2O + CO2 + 2NH3 = CaCO3 + 2NH4Cl。(7)a、b、c装置均起不到防倒吸的作用,只有b装置可以。
Ⅱ.
(1)、(2)从流程图可以看出在加入试剂A之后,出现浊液,而且浊液经过操作B能够得到沉淀,这说明加入的试剂A是一种能够与NaHCO3发生化学反应产生沉淀的试剂,经分析,这种试剂应当是一种能够与NaHCO3发生反应的强碱,如Ca(OH)2或Ba(OH)2,由此不难得出结论,操作B应当是过滤操作,计算如下:
根据C原子守恒可知:
NaHCO3—CaCO3
84 100

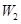
NaHCO3—BaCO3
84 197
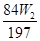
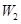
因此,样品中氯化铵的质量分数为: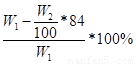 或
或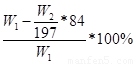 。
。
考点:考查二氧化碳和氨气的实验室制法、化学实验基本操作、化学方程式的书写、化学实验安全防倒吸装置的识别与判断、物资的分离与提纯、化学计算。

 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案