题目内容
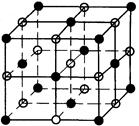
NaCl的晶胞如右图,每个NaCl晶胞中含有的Na+离子和Cl
 离子的数目分别是( )
离子的数目分别是( )
| A.14,13 | B.1,1 | C.4,4 | D.6,6 |
答案:C
每个NaCl晶胞中含有的Na+离子和Cl
 离子的数目分别是4、4。
离子的数目分别是4、4。
练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
题目内容

 离子的数目分别是( )
离子的数目分别是( )
| A.14,13 | B.1,1 | C.4,4 | D.6,6 |
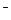 离子的数目分别是4、4。
离子的数目分别是4、4。
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案