题目内容
【题目】氢氧化铁胶体的制备与其性质检验实验如下,请回答下列问题。
(1)写出制备氢氧化铁胶体的化学方程式_____。
(2)制备实验操作:取一小烧杯加入25mL蒸馏水加热至沸腾,向沸水中逐滴加入1~2mL____,继续煮沸至___,停止加热。
(3)证明有氢氧化铁胶体生成的实验操作是______。
(4)若取少量制得的胶体加入试管中,加入硫酸铵溶液,现象是___,这种现象称为胶体的____。
【答案】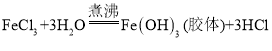 氯化铁饱和溶液 混合液呈红褐色 让一束可见光通过制得的液体,从侧面观察到一条光亮的“通路”,说明制得的是胶体 产生红褐色沉淀 聚沉
氯化铁饱和溶液 混合液呈红褐色 让一束可见光通过制得的液体,从侧面观察到一条光亮的“通路”,说明制得的是胶体 产生红褐色沉淀 聚沉
【解析】
(1)写出制备氢氧化铁胶体的化学方程式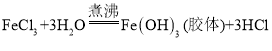 ;
;
(2)氢氧化铁胶体制备:将饱和氯化铁溶液滴入沸水中,继续煮沸至溶液呈红褐色,停止加热;
(3)胶体有丁达尔效应,让一束可见光通过制得的液体,从侧面观察到一条光亮的“通路”,说明制得的是胶体;
(4)当向氢氧化铁胶体中加入电解质硫酸铵溶液时,氢氧化铁胶粒发生聚沉,产生红褐色沉淀。

 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案【题目】[化学-选修2:化学与技术]
双氧水是一种重要的氧化剂、漂白剂和消毒剂。生产双氧水常采用蒽醌法,其反应原理和生产流程如图所示:


A.氢化釜 | B.过滤器 | C.氧化塔 | D.萃取塔E.净化塔F.工作液再生装置G.工作液配制装置 |
生产过程中,把乙基蒽醌溶于有机溶剂配制成工作液,在一定的温度、压力和催化剂作用下进行氢化,再经氧化、萃取、净化等工艺得到双氧水。回答下列问题:
(1)蒽醌法制备双氧水理论上消耗的原料是_______,循环使用的|原料是______,配制工作液时采用有机溶剂而不采用水的原因是______。
(2)氢化釜A中反应的化学方程式为_______,进入氧化塔C的反应混合液中的主要溶质为_______。
(3)萃取塔D中的萃取剂是____,选择其作萃取剂的原因是______。
(4)工作液再生装置F中要除净残留的H2O2,原因是______。
(5)双氧水浓度可在酸性条件下用KMnO4溶液测定,该反应的离子方程式为_______。一种双氧水的质量分数为27.5%,(密度为1.10g·cm3),其浓度为______mol/L。
【题目】[2016·新课标I]锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)基态Ge原子的核外电子排布式为[Ar]_______________,有__________个未成对电子。
(2)Ge与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键。从原子结构角度分析,原因是______________________________。
(3)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因______________________________。
GeCl4 | GeBr4 | GeI4 | |
熔点/℃ | 49.5 | 26 | 146 |
沸点/℃ | 83.1 | 186 | 约400 |
(4)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是______________________________。
(5)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为_______________,微粒之间存在的作用力是_______________。
(6)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置。如图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为(![]() ,0,
,0,![]() );C为(
);C为(![]() ,
,![]() ,0)。则D原子的坐标参数为_______________。
,0)。则D原子的坐标参数为_______________。

②晶胞参数,描述晶胞的大小和形状。已知Ge单晶的晶胞参数a=565.76 pm,其密度为_____g·cm3(列出计算式即可)。



