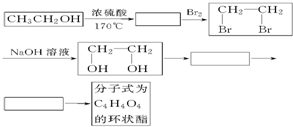
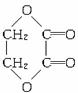
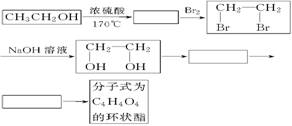
��Ŀ����
�����ִ���ҵ�ķ�չ����Դ�����Ѿ�Խ��Խ�������ǵ����ӣ���ѧ��Ԥ�ԣ�δ���������ȼ������ɫֲ�����ֲ��Ľոѣ���Ҫ�ɷ�����ά�أ����ʵ��Ĵ�������ˮ��������ǣ��ٽ�������ת��Ϊ�Ҵ�������ȼ�ϣ�
��1��д����ɫֲ��Ľո�ת��Ϊ�������Լ��Ҵ�����ȼ�ϵĻ�ѧ����ʽ��
��
��2���ֱ�ȡ1mol�����ǽ�������ʵ�飺
���������ڼ��ԡ����������£�����������Һ��Ӧ����
������ᷴӦ���������������Ͻ���ȫ������
����ʹ֮ȫ��ת��ΪCO2��H2O����������������ڱ�״����Ϊ
�������Ƶ�Cu��OH��2�ڼ��ȵ������·�Ӧ��������
��1��д����ɫֲ��Ľո�ת��Ϊ�������Լ��Ҵ�����ȼ�ϵĻ�ѧ����ʽ��
��
��C6H10O5��n ����ά�أ�+nH2O
nC6H12O6��������
| ���� |
| �� |
��C6H10O5��n ����ά�أ�+nH2O
nC6H12O6��������
����| ���� |
| �� |
C2H5OH+3O2
2CO2+3H2O
| ��ȼ |
C2H5OH+3O2
2CO2+3H2O
��| ��ȼ |
��2���ֱ�ȡ1mol�����ǽ�������ʵ�飺
���������ڼ��ԡ����������£�����������Һ��Ӧ����
��
��
���˷�Ӧ�������ƾ���ҵ��������ᷴӦ���������������Ͻ���ȫ������
300
300
g���ᣮ����ʹ֮ȫ��ת��ΪCO2��H2O����������������ڱ�״����Ϊ
134.4
134.4
L����Ӧ�Ļ�ѧ����ʽΪC6H12O6+6O2��6CO2+6H2O��
C6H12O6+6O2��6CO2+6H2O��
�������Ƶ�Cu��OH��2�ڼ��ȵ������·�Ӧ��������
������ɫ����
������ɫ����
����������1��������ά�ص�ˮ��õ������ǣ��Ҵ���һ�ֱȽ�������Դ��ȼ�����ɶ�����̼��ˮ��
��2���ٸ����������ڼ��ԡ����������£��ܱ�������Һ�������ɵ�������
�ڸ�������������ᷴӦ�ķ���ʽ���м��㣻
�۸��������ǵ�������Ӧ�����㣻
�ܸ��������������Ƶ�Cu��OH��2��Ӧ����ש��ɫ��������ͭ������
��2���ٸ����������ڼ��ԡ����������£��ܱ�������Һ�������ɵ�������
�ڸ�������������ᷴӦ�ķ���ʽ���м��㣻
�۸��������ǵ�������Ӧ�����㣻
�ܸ��������������Ƶ�Cu��OH��2��Ӧ����ש��ɫ��������ͭ������
����⣺��1����ά���ڴ�����������������ˮ�����������ǣ���C6H10O5��n����ά�أ�+nH2O
nC6H12O6�������ǣ���
�Ҵ���һ�ֱȽ�������Դ��ȼ�����ɶ�����̼��ˮ��C2H5OH+3O2
2CO2+3H2O��
�ʴ�Ϊ����C6H10O5��n ����ά�أ�+nH2O
nC6H12O6�������ǣ���C2H5OH+3O2
2CO2+3H2O��
��2�����������ڼ��ԡ����������£��ܱ�������Һ�������ɵ�������������Һ��Ӧ���������˷�Ӧ�������ƾ���ҵ���ʴ�Ϊ������
��������������ᷴӦ�������ķ���ʽΪ��CH2OH��CHOH��4CHO+5CH3COOH��CH3COOCH2��CH3COOCH��4CHO+5H2O��1mol�����Dzμӷ�Ӧ����Ҫ5mol���ᣬ������Ϊ��5mol��60g/mol=300g���ʴ�Ϊ��300��
���������������ڻ���������C6H12O6+6O2��6CO2+6H2O��1mol�����Dzμӷ�Ӧ����Ҫ6mol�����������Ϊ��6mol��22.4L/mol=134.4L��
�ʴ�Ϊ��134.4��C6H12O6+6O2��6CO2+6H2O��
���������������Ƶ�Cu��OH��2��Ӧ����ש��ɫ��������ͭ��������������Ϊ����ש��ɫ������
�ʴ�Ϊ������ש��ɫ������
| ���� |
| �� |
�Ҵ���һ�ֱȽ�������Դ��ȼ�����ɶ�����̼��ˮ��C2H5OH+3O2
| ��ȼ |
�ʴ�Ϊ����C6H10O5��n ����ά�أ�+nH2O
| ���� |
| �� |
| ��ȼ |
��2�����������ڼ��ԡ����������£��ܱ�������Һ�������ɵ�������������Һ��Ӧ���������˷�Ӧ�������ƾ���ҵ���ʴ�Ϊ������
��������������ᷴӦ�������ķ���ʽΪ��CH2OH��CHOH��4CHO+5CH3COOH��CH3COOCH2��CH3COOCH��4CHO+5H2O��1mol�����Dzμӷ�Ӧ����Ҫ5mol���ᣬ������Ϊ��5mol��60g/mol=300g���ʴ�Ϊ��300��
���������������ڻ���������C6H12O6+6O2��6CO2+6H2O��1mol�����Dzμӷ�Ӧ����Ҫ6mol�����������Ϊ��6mol��22.4L/mol=134.4L��
�ʴ�Ϊ��134.4��C6H12O6+6O2��6CO2+6H2O��
���������������Ƶ�Cu��OH��2��Ӧ����ש��ɫ��������ͭ��������������Ϊ����ש��ɫ������
�ʴ�Ϊ������ש��ɫ������
������������Ҫ�����������ǵ���Դ�����ʣ��ѶȲ���ץס�����ŵ������ǽ���Ĺؼ���

��ϰ��ϵ�д�
�����Ŀ
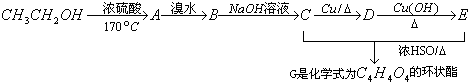
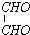
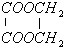
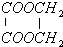 +2H2O
+2H2O