题目内容
关于原电池的叙述正确的是( )
| A.原电池工作时,电极上不一定都发生氧化还原反应 |
B.某可逆电池充、放电时的反应式为Li1-xNiO2+xLi LiNiO2,放电时此电池的负极材料是Li1-xNiO2 LiNiO2,放电时此电池的负极材料是Li1-xNiO2 |
| C.铅、银和盐酸构成的原电池工作时,铅板上有5.175 g铅溶解,正极上就有1 120 mL(标准状况)气体析出 |
| D.在理论上可将反应CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH<0设计成原电池 |
D
解析

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
如图为一种微生物燃料电池结构示意图,关于该电池叙述正确的是
| A.分子组成为Cm(H2O)n的物质一定是糖类 |
| B.微生物所在电极区放电时发生还原反应 |
| C.放电过程中,H+从正极区移向负极区 |
| D.正极反应式为:MnO2+4H++2e—=Mn2++2H2O |
[双选题]烧杯A中盛放0.1 mol·L-1的H2SO4溶液,烧杯B中盛放0.1 mol·L-1的
CuCl2溶液(两种溶液均足量),装置如图所示,下列说法不正确的是( )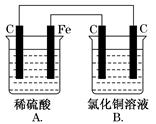
| A.A为原电池,B为电解池 |
| B.A为电解池,B为原电池 |
| C.当A烧杯中产生0.1 mol气体时,B烧杯中产生气体的物质的量也为0.1 mol |
| D.一段时间后,B烧杯中溶液的浓度增大 |
新型LiFePO4可充电锂离子动力电池以其独特的优势成为绿色能源的新宠。已知该电池放电时的电极反应为:正极:FePO4+Li++e- LiFePO4,负极:Li-e-
LiFePO4,负极:Li-e- Li+。下列说法中正确的是( )
Li+。下列说法中正确的是( )
| A.充电时动力电池上标注“+”的电极应与外接电源的正极相连 |
B.放电时电池反应为FePO4+Li++e- LiFePO4 LiFePO4 |
| C.放电时电池内部Li+向负极移动 |
| D.放电时,在正极上Li+得电子被还原 |
有一种锂电池,用金属锂和石墨作电极材料,电解质溶液是由四氯铝锂(LiAlCl4)溶解在亚硫酰氯(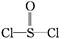 )中而形成的,电池总反应方程式为:8Li+3SOCl2
)中而形成的,电池总反应方程式为:8Li+3SOCl2 6LiCl+Li2SO3+2S,下列叙述中正确的是( )
6LiCl+Li2SO3+2S,下列叙述中正确的是( )
| A.电解质溶液中混入水,对电池反应无影响 |
| B.金属锂作电池的正极,石墨作电池的负极 |
| C.电池工作过程中,亚硫酰氯(SOCl2)被还原为Li2SO3 |
| D.电池工作过程中,金属锂提供的电子与正极区析出硫的物质的量之比为4∶1 |
电解100 mL含c(H+)=0.30 mol·L-1下列溶液,当电路中通过0.04 mol
电子时,理论上析出金属质量最大的是( )
| A.0.10 mol·L-1AgNO3溶液 |
| B.0.10 mol·L-1ZnSO4溶液 |
| C.0.20 mol·L-1CuCl2溶液 |
| D.0.20 mol·L-1Pb(NO3)2溶液 |
已知298 K时,Mg(OH)2的溶度积常数Ksp=5.6×10-12,取适量的MgCl2溶液,加入一
定量的烧碱溶液达到沉淀溶解平衡,测得pH=13,则下列说法不正确的是( )
| A.所得溶液中的c(H+)=1.0×10-13 mol·L-1 |
| B.所得溶液中由水电离产生的c(OH-)=1.0×10-13 mol·L-1 |
| C.所加的烧碱溶液的pH=13.0 |
| D.所得溶液中的c(Mg2+)=5.6×10-10 mol·L-1 |
某新型电池,以NaBH4(B的化合价为+3)和H2O2作原料,该电池可用作深水勘探等无空气环境电源,其工作原理如图所示。下列说法正确的是 ( )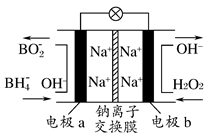
| A.电池工作时Na+从b极区移向a极区 |
| B.每消耗3 mol H2O2,转移3 mol e- |
| C.b极上的电极反应式为:H2O2+2e-+2H+=2H2O |
| D.a极上的电极反应式为:BH4—+8OH--8e-=BO2—+6H2O |
