题目内容
【题目】(8分)通过粮食发酵可获得某含氧有机化合物X,其相对分子质量为46,其中碳的质量分数为52.2%,氢的质量分数为13.0%。
(1)X的分子式是(写出计算过程) 。
(2)X与金属钠反应放出氢气,反应的化学方程式是 。
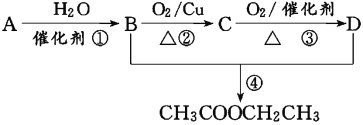
(3)X与空气中的氧气在铜或银催化下反应生成Y,Y的结构简式是 。
(4)X与酸性高锰酸钾溶液反应可生成Z,在加热和浓硫酸作用下,X与Z反应可生成一种有香味的物质W。若184 g X和120 g Z反应能生成106 g W,计算该反应的产率(实际产量与理论产量之比) 。
【答案】(1)C2H6O(2分) (2)2Na+2CH3CH2OH→2CH3CH2ONa+H2↑(3分)
(3)CH3CHO(2分) (4)60.2%(3分)
【解析】试题(1)根据题意X的分子中含碳原子数为![]() ≈2,含氢原子数为
≈2,含氢原子数为![]() ≈6,含氧原子数为
≈6,含氧原子数为![]() ≈1,所以X的分子式为C2H6O。
≈1,所以X的分子式为C2H6O。
(2)X与金属钠反应放出氢气,则X是乙醇,反应的化学方程式是2Na+2CH3CH2OH→2CH3CH2ONa+H2↑。
(3)X与空气中的氧气在铜或银催化下反应生成Y,Y是乙醛,结构简式是CH3CHO。
(4)X与酸性高锰酸钾溶液反应可生成Z,在加热和浓硫酸作用下,X与Z反应可生成一种有香味的物质W,所以Z是乙酸,W是乙酸乙酯。若184 g X和120 g Z反应能生成106 g W,其中乙醇是184g÷46g/mol=4mol,乙酸是120g÷60g/mol=2mol,则理论上应该生成2mol乙酸乙酯,质量是2mol×88g/mol=176g。所以该反应的产率=![]() 。
。

练习册系列答案
 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案
相关题目