题目内容
TiO2既是制备其他含钛化合物的原料,又是一种性能优异的白色颜料。
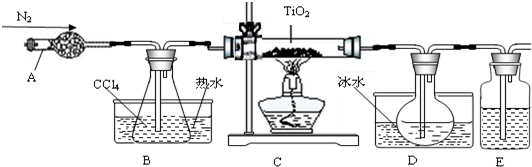
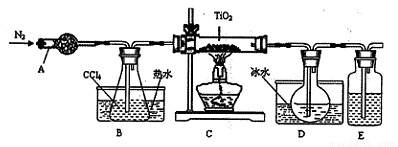
(1)实验室利用反应TiO2(s)+2CCl4(g)=TiCl4(g)+CO2(g),在无水无氧条件下,制取TiCl4实验装置示意图如下??
有关性质如下表???
物质 | 熔点/℃ | 沸点/℃ | 其它 |
CCl4 | -23 | 76 | 与 TiCl4互溶 |
TiCl4 | -25 | 136 | 遇潮湿空气产生白雾 |
仪器A的名称是____???? ,装置E中的试剂是????????? 。反应开始前必须进行的操作是____???? ;反应结束后的操作包括:①停止通氮气②熄灭酒精灯③冷却至室温。正确的顺序为____???? (填序号)。欲分离D中的液态混合物,所采用操作的名称是????????? 。
(2)工业上由钛铁矿(FeTO3)(含Fe2O3、SiO2等杂质)制备TiO2的有关反应包括:
酸溶:FeTiO3(s)+2H2SO4(aq)??? FeSO4(aq)+TiOSO4(aq)+2H2O(1)
水解;TiOSO4(aq)+2H2O(1)??? H2T1O3(s)+H2SO4(aq)
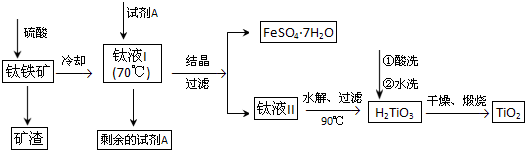
简要工艺流程如下:
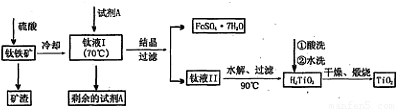
①试剂A为??????????? 。钛液I需冷却至70℃左右,若温度过高会导致产率降低,原因是????????? 。
②取少量酸洗后的H2TiO3,加入盐酸并振荡,滴加KSCN溶液后无明显现象,再加H2O2后出现微红色,说明H2TiO3中存在的杂质离子是____??????? ,写出其中发生氧化还原反应的离子方程式____??? 。这种H2TiO3即使用水充分洗涤,煅烧后获得的TiO2也会发黄,发黄的杂质是____???????? (填化学式)。
(1)(球形)干燥管?? 浓硫酸? 检查装置的气密性?? ②③①??? 蒸馏
(2)①铁粉? 由于TiOSO4容易水解,若温度过高,则会有较多TiOSO4水解为固体H2TiO3而经过滤进入FeSO4·7H2O中导致TiO2产率降低。②Fe2+?? H2O2+2Fe2++2H+=2Fe3++2H2O??? Fe2O3
【解析】
 试题分析:(1)仪器A的名称是球形干燥管,仪器B的作用是加热CCl4,使整个装置充满四氯化碳蒸汽。任何有气体参加的反应或制备气体的反应,在反应开始前都要检查装置的气密性。反应结束后为了防止TiCl4潮解,正确的操作顺序是②熄灭酒精灯③冷却至室温 ①停止通氮气 。TiCl4和CCl4的混合物,因为它们是沸点不同的、互溶的液态混合物,所以分离二者的方法是蒸馏。(2)①在钛铁矿FeTO3中含有Fe2O3、SiO2等杂质。在加入H2SO4时钛铁矿及Fe2O3溶解在其中,不能溶解的SiO2通过过滤分离除去。在滤液中含有Fe2 (SO4)3,为了制取纯净的绿矾,要在钛液中加入Fe粉把Fe2 (SO4)3还原为FeSO4。由于TiOSO4容易水解,若温度过高,则会有较多TiOSO4水解为固体H2TiO3而经过滤进入FeSO4·7H2O中导致TiO2产率降低。②滴加KSCN溶液后无明显现象,再加H2O2后出现微红色,说明H2TiO3中存在的杂质离子是Fe2+。其中发生氧化还原反应的离子方程式H2O2+2Fe2++2H+=2Fe3++2H2O。在H2TiO3受热分解时,其中的杂质Fe(OH)3也发生了分解反应:2Fe(OH)3
试题分析:(1)仪器A的名称是球形干燥管,仪器B的作用是加热CCl4,使整个装置充满四氯化碳蒸汽。任何有气体参加的反应或制备气体的反应,在反应开始前都要检查装置的气密性。反应结束后为了防止TiCl4潮解,正确的操作顺序是②熄灭酒精灯③冷却至室温 ①停止通氮气 。TiCl4和CCl4的混合物,因为它们是沸点不同的、互溶的液态混合物,所以分离二者的方法是蒸馏。(2)①在钛铁矿FeTO3中含有Fe2O3、SiO2等杂质。在加入H2SO4时钛铁矿及Fe2O3溶解在其中,不能溶解的SiO2通过过滤分离除去。在滤液中含有Fe2 (SO4)3,为了制取纯净的绿矾,要在钛液中加入Fe粉把Fe2 (SO4)3还原为FeSO4。由于TiOSO4容易水解,若温度过高,则会有较多TiOSO4水解为固体H2TiO3而经过滤进入FeSO4·7H2O中导致TiO2产率降低。②滴加KSCN溶液后无明显现象,再加H2O2后出现微红色,说明H2TiO3中存在的杂质离子是Fe2+。其中发生氧化还原反应的离子方程式H2O2+2Fe2++2H+=2Fe3++2H2O。在H2TiO3受热分解时,其中的杂质Fe(OH)3也发生了分解反应:2Fe(OH)3 Fe2O3+3H2O 。分解产生的Fe2O3混在TiO2使物质发黄。
Fe2O3+3H2O 。分解产生的Fe2O3混在TiO2使物质发黄。
考点:考查仪器的辨认、装置气密性的检查、实验的顺序、杂质的检验与除去、混合物的分离及盐的水解。

 优等生题库系列答案
优等生题库系列答案(15分)TiO2既是制备其他含钛化合物的原料,又是一种性能优异的白色颜料。
(1)实验室利用反应TiO2(s)+2CCl4(g)==TiCl4(g)+CO2(g),在无水无氧条件下,制取TiCl4实验装置示意图如下

有关性质如下表
| 物质 | 熔点/℃ | 沸点/℃ | 其他 |
| CCl4 | -23 | 76 | 与TiCl4互溶 |
| TiCl4 | -25 | 136 | 遇潮湿空气产生白雾 |
仪器A的名称是 ,装置E中的试剂是 。反应开始前依次进行如下操作:①停止通氮气②熄灭酒精灯③冷却至室温。正确的顺序为 (填序号)。欲分离D中的液态混合物,所采用操作的名称是 。
(2)工业上由钛铁矿(FeTiO3)(含Fe2O3、SiO2等杂质)制备TiO2的有关反应包括:
酸溶FeTiO3(s)+2H2SO4(aq)==FeSO4(aq)+ TiOSO4(aq)+ 2H2O(l)
水解TiOSO4(aq)+ 2H2O(l)=90℃= H2TiO3(s)+H2SO4(aq)
简要工艺流程如下:①试剂A为 。钛液Ⅰ需冷却至70℃左右,若温度过高会导致产品收率降低,原因是
②取少量酸洗后的H2TiO3,加入盐酸并振荡,滴加KSCN溶液后无明显现象,再加H2O2后出现微红色,说明H2TiO3中存在的杂质离子是 。这种H2TiO3即使用水充分洗涤,煅烧后获得的TiO2也会发黄,发黄的杂质是 (填化学式)。
TiO2既是制备其他含钛化合物的原料,又是一种性能优异的白色颜料。
(1)实验室利用反应TiO2(s)+CCl4(g) TiCl4(g)+CO2(g),在无水无氧条件下制备TiCl4,实验装置示意图如下:
TiCl4(g)+CO2(g),在无水无氧条件下制备TiCl4,实验装置示意图如下: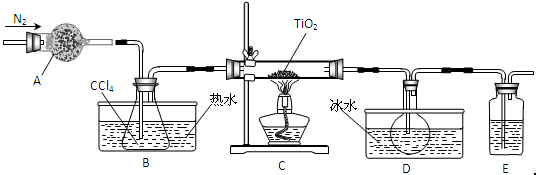
有关物质性质如下表
| 物质 | 熔点/℃ | 沸点/℃ | 其他 |
| CCl4 | -23 | 76 | 与TiCl4互溶 |
| TiCl4 | -25 | 136 | 遇潮湿空气产生白雾 |
仪器A的名称是 ,装置E中的试剂是 。反应开始前依次进行如下操作:组装仪器、 、加装药品、通N2一段时间后点燃酒精灯。反应结束后的操作包括:①停止通N2 ②熄灭酒精灯 ③冷却至室温。正确的顺序为 (填序号)。欲分离D中的液态混合物,所采用操作的名称是 。
(2)工业上由钛铁矿(FeTiO3)(含Fe2O3、SiO2等杂质)制备TiO2的有关反应包括:
酸溶 FeTiO3(s)+2H2SO4(aq)=FeSO4(aq)+ TiOSO4(aq)+ 2H2O(l)
水解 TiOSO4(aq)+ 2H2O(l)
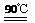 H2TiO3(s)+H2SO4(aq)
H2TiO3(s)+H2SO4(aq) 简要工艺流程如下:
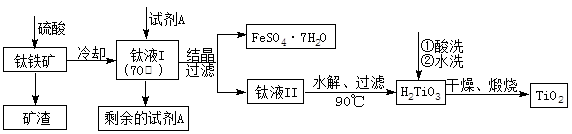
①试剂A为 。钛液Ⅰ需冷却至70℃左右,若温度过高会导致产品TiO2收率降低,原因是 。
②取少量酸洗后的H2TiO3,加入盐酸并振荡,滴加KSCN溶液后无明显现象,再加H2O2后出现微红色,说明H2TiO3中存在的杂质离子是 。这种H2TiO3即使用水充分洗涤,煅烧后获得的TiO2也会发黄,发黄的杂质是 (填化学式)。
TiO2既是制备其他含钛化合物的原料,又是一种性能优异的白色颜料。
(1)实验室利用反应TiO2(s)+CCl4(g) TiCl4(g)+CO2(g),在无水无氧条件下制备TiCl4,实验装置示意图如下:
TiCl4(g)+CO2(g),在无水无氧条件下制备TiCl4,实验装置示意图如下:
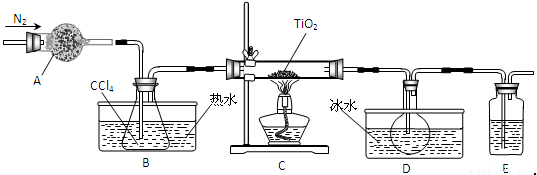
有关物质性质如下表
|
物质 |
熔点/℃ |
沸点/℃ |
其他 |
|
CCl4 |
-23 |
76 |
与TiCl4互溶 |
|
TiCl4 |
-25 |
136 |
遇潮湿空气产生白雾 |
仪器A的名称是 ,装置E中的试剂是 。反应开始前依次进行如下操作:组装仪器、 、加装药品、通N2一段时间后点燃酒精灯。反应结束后的操作包括:①停止通N2 ②熄灭酒精灯 ③冷却至室温。正确的顺序为 (填序号)。欲分离D中的液态混合物,所采用操作的名称是 。
(2)工业上由钛铁矿(FeTiO3)(含Fe2O3、SiO2等杂质)制备TiO2的有关反应包括:
酸溶 FeTiO3(s)+2H2SO4(aq)=FeSO4(aq)+ TiOSO4(aq)+ 2H2O(l)
水解
TiOSO4(aq)+ 2H2O(l) H2TiO3(s)+H2SO4(aq)
H2TiO3(s)+H2SO4(aq)
简要工艺流程如下:
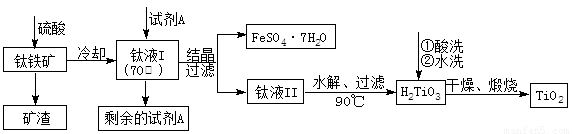
①试剂A为 。钛液Ⅰ需冷却至70℃左右,若温度过高会导致产品TiO2收率降低,原因是 。
②取少量酸洗后的H2TiO3,加入盐酸并振荡,滴加KSCN溶液后无明显现象,再加H2O2后出现微红色,说明H2TiO3中存在的杂质离子是 。这种H2TiO3即使用水充分洗涤,煅烧后获得的TiO2也会发黄,发黄的杂质是 (填化学式)。