题目内容
在密闭容器中,对于可逆反应A+3B

2C(g),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是( )
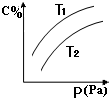

2C(g),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是( )
| A.A一定为气体 |
| B.B一定为气体 |
| C.该反应是放热反应 |
| D.若正反应方向△H<0,则T1>T2 |

A、当温度一定时,压强越大,化学平衡向气体体积减小的方向移动,C的含量越大,说明平衡向正反应方向移动,所以该反应是一个反应前后气体体积减小的化学反应,即B一定是气体,A可能是气体,故A错误.
B、当温度一定时,压强越大,化学平衡向气体体积减小的方向移动,C的含量越大,说明平衡向正反应方向移动,所以该反应是一个反应前后气体体积减小的化学反应,即B一定是气体,故B正确.
C、当压强一定时,如果T1>T2,升高温度,平衡向吸热反应方向移动,C的含量增大,说明正反应是吸热反应;如果T2>T1,升高温度,平衡向吸热反应方向移动,C的含量降低,说明正反应是放热反应,T2和T1的大小未知,所以无法判断该反应是放热反应还是吸热反应,故C错误.
D、若正反应方向△H<0,升高温度,平衡向逆反应方向移动导致C的含量减小,则T1<T2,故D错误.
故选B.
B、当温度一定时,压强越大,化学平衡向气体体积减小的方向移动,C的含量越大,说明平衡向正反应方向移动,所以该反应是一个反应前后气体体积减小的化学反应,即B一定是气体,故B正确.
C、当压强一定时,如果T1>T2,升高温度,平衡向吸热反应方向移动,C的含量增大,说明正反应是吸热反应;如果T2>T1,升高温度,平衡向吸热反应方向移动,C的含量降低,说明正反应是放热反应,T2和T1的大小未知,所以无法判断该反应是放热反应还是吸热反应,故C错误.
D、若正反应方向△H<0,升高温度,平衡向逆反应方向移动导致C的含量减小,则T1<T2,故D错误.
故选B.

练习册系列答案
 优生乐园系列答案
优生乐园系列答案
相关题目
一定条件下,工业上制取氨的反应为N2+3H2?2NH3.对于在密闭容器中进行的该反应,下列说法正确的是( )
| A、使用合适的催化剂,可使N2和H2都全部变成NH3 | B、达到平衡状态时,NH3的浓度一定是N2的2倍 | C、增大N2的浓度可使H2的转化率达到100% | D、反应不能进行到底,有一定的限度 |

 CH3OH(g)+H2O(g) △H = —49.0 kJ·mol-1
CH3OH(g)+H2O(g) △H = —49.0 kJ·mol-1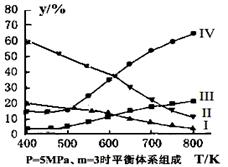
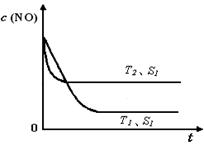
 2CO2(g)+ N2(g) 中NO的浓度随温度(T)、催化剂表面积(S)和时间(t)的变化曲线,若催化剂的表面积S1>S2 ,在上图中画出NO的浓度在T1、S2 条件下达到平衡过程中的变化曲线,并注明条件。
2CO2(g)+ N2(g) 中NO的浓度随温度(T)、催化剂表面积(S)和时间(t)的变化曲线,若催化剂的表面积S1>S2 ,在上图中画出NO的浓度在T1、S2 条件下达到平衡过程中的变化曲线,并注明条件。 CH3OH(g)+H2O(g)
△H = —49.0 kJ·mol-1
CH3OH(g)+H2O(g)
△H = —49.0 kJ·mol-1 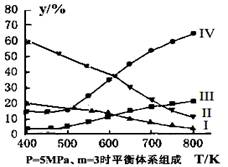
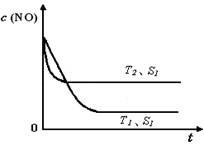
 2CO2(g)+ N2(g) 中NO的浓度随温度(T)、催化剂表面积(S)和时间(t)的变化曲线, 若催化剂的表面积S1>S2 ,在上图中画出NO的浓度在T1、S2 条件下达到平衡过程中的变化曲线,并注明条件。
2CO2(g)+ N2(g) 中NO的浓度随温度(T)、催化剂表面积(S)和时间(t)的变化曲线, 若催化剂的表面积S1>S2 ,在上图中画出NO的浓度在T1、S2 条件下达到平衡过程中的变化曲线,并注明条件。