题目内容
用标准盐酸滴定未知浓度的NaOH溶液,下列各操作中,不会引起实验误差的是
| A.用蒸馏水冼净滴定管后,装入标准盐酸进行滴定 |
| B.用蒸馏水冼净锥形瓶后,再用NaOH液润洗,而后装入一定体积的NaOH溶液 |
| C.用甲基橙做指示剂,当溶液由黄色变成橙色,立刻读数盐酸体积 |
| D.用碱式滴定管取10.00 mLNaOH溶液放入用蒸馏水洗净的锥形瓶中,再加入适量蒸馏水进行滴定 |
D
解析试题分析:根据C测=C标V标/V测来分析对V(标)的影响。用蒸馏水冼净滴定管后,装入标准盐酸进行滴定,相当于盐酸的浓度被稀释,则消耗盐酸的体积增加,测定结果偏高;用蒸馏水冼净锥形瓶后,再用NaOH液润洗,而后装入一定体积的NaOH溶液,相当于是增加了氢氧化钠的物质的量,则消耗盐酸的体积增加,测定结果偏高;用甲基橙做指示剂,当溶液由黄色变成橙色,并在半分钟内不褪色,如果立刻读数盐酸体积,则测定结果偏低;选项D中加入适量的蒸馏水后,氢氧化钠的物质的量不变,则为消耗盐酸的体积不变,测定结果不变,答案选D。
考点:考查中和滴定实验中误差分析的有关判断
点评:该题是高考中的常见题型和重要的考点,侧重对学生实验分析以及评价的考查,有利于激发学生的学习兴趣和学习积极性。该题的关键是明确滴定误差分析的判断依据,即误差分析的总依据为:由C测=C标V标/V测,由于C标、V待均为定植,所以C测的大小取决于V标的大小,即V标:偏大或偏小,则C测偏大或偏小。

练习册系列答案
 字词句段篇系列答案
字词句段篇系列答案
相关题目
 (2012?江苏一模)下列有关实验原理或操作正确的是( )
(2012?江苏一模)下列有关实验原理或操作正确的是( )
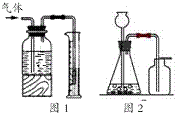 下列有关实验原理或操作正确的是
下列有关实验原理或操作正确的是