题目内容
(10分)短周期元素A、B、C、D、E的原子序数依次增大,已知:
①C的最高价氧化物对应的水化物与其气态氢化物反应可生成盐;
②A的氧化物是生活中最常见液体,A、E同主族,C与B、D相邻;
③A、B、C、D四种元素组成一种离子化合物F,1 molF中含有10mol原子。
请回答下列问题:
(1)C的气态氢化物的电子式为 ,A在周期表中的位置
(2)化合物E2D2中阴阳离子个数比为 ,F含有的化学键类型为
(3)F溶液与足量EDA的稀溶液混合,其离子方程式为
(4)氯气与C的气态氢化物相遇有白烟及C2生成,写出其化学反应方程式并用单线桥表示电子转移的方向和数目
(5)将A2、D2分别充人多孔性石墨电极,将电极插入EDA的水溶液中构成原电池,负极的电极反应为 ;一段时间后EDA的浓度将 (填“变大”、“变小”、“不变”或“无法确定”)。
(10分)
(1)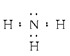 ;第一周期、第IA族
;第一周期、第IA族
(2)1:2;离子键和共价键
(3)2OH-+HCO3-+NH4+=CO32-+H2O+NH3·H2O(2分)
(4) 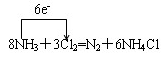 (2分)
(2分)
(5)H2-2e-+2OH-=2H2O;变小(其他每空1分)
解析

练习册系列答案
 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案
相关题目

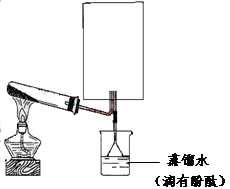

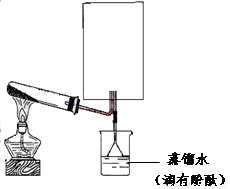
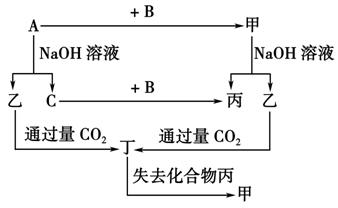
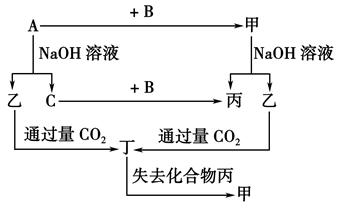
 ___________________________
___________________________